题目内容
对于反应2SO3(g)(1)若保持压强、温度不变,向该容器里再通入1 mol SO2和0.5 mol O2,则平衡时SO3的含量___________A%(填“大于”“等于”或“小于”,下同)。
(2)若保持压强、温度不变,向该容器里通入1 mol N2,则平衡时SO3的含量________A%。
(3)若保持体积、温度不变,向该容器中通入1 mol N2,则平衡时SO3的含量________A%。
(4)若保持体积不变,温度升高100 ℃,此温度下容器内的压强____p,平衡向_____方向移动。
(1)等于 (2)小于 (3)等于 (4)大于 正反应
解析:(1)压强、温度不变,按方程式中反应物或生成物的化学计量数之比添加物质,重新达到平衡时各物质的含量保持不变;(2)保持压强、温度不变,向容器中通入N2,反应混合物的分压减小,容器的体积增大,平衡向正反应方向移动,SO3的含量降低;(3)体积、温度不变,向容器中通入N2,虽然容器内总压增大,但反应混合物的分压不变,平衡不移动;(4)体积不变,升高温度,平衡正向移动,反应混合物总物质的量增大,压强增大。

练习册系列答案
相关题目
|
对于反应2SO3(g) | |
| [ ] | |
A. |
2体积SO2和足量O2反应,必定生成2体积SO3 |
B. |
其他条件不变,增大压强,化学反应速率必定增大 |
C. |
平衡时,SO2的消耗速率必定等于O2的生成速率 |
D. |
平衡时,SO2浓度必定等于O2浓度的2倍 |
对于反应2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )
| A.通入大量O2,V正增大,V逆减小 |
| B.2V正(SO2) =V逆(O2)时,反应达到平衡 |
| C.恒温恒容充入Ne,容器内压强增大,V正、V逆均不变 |
| D.V (SO2)∶V (O2)∶V (SO3) =2∶1∶2时,反应达到平衡 |
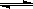 2SO3(g)能增大正反应速率的措施是
2SO3(g)能增大正反应速率的措施是