题目内容
足量Cu溶于浓HNO3,产生NO2、N2O4、NO气体,这些气体若与2.24LO2(标况)混合后通入水中,气体被完全吸收,若向原所得溶液中加入0.1mol/L-1H2SO4溶液100mL,则继续溶解的Cu质量为 .
考点:化学方程式的有关计算
专题:
分析:Cu和浓硝酸反应过程中,Cu失电子生成铜离子、硝酸得电子生成NO2、N2O4、NO,且转移电子守恒,这些气体若与2.24LO2(标况)混合后通入水中,气体被完全吸收,说明氧气得到的电子等于这些气体生成硝酸根离子得到的电子,所以氧气得到的电子等于Cu失去的电子,根据转移电子守恒得到硝酸铜的物质的量,再根据离子方程式计算加入稀硫酸后溶解的Cu.
解答:
解:Cu和浓硝酸反应过程中,Cu失电子生成铜离子、硝酸得电子生成NO2、N2O4、NO,且转移电子守恒,这些气体若与2.24LO2(标况)混合后通入水中,气体被完全吸收,说明氧气得到的电子等于这些气体生成硝酸根离子得到的电子,所以氧气得到的电子等于Cu失去的电子,根据转移电子得n(Cu)=
=0.2mol,根据原子守恒得n(Cu)=n[Cu(NO3)2]=0.2mol,再加入稀硫酸后,相当于溶液中含有硝酸,能继续溶解Cu,n(H+)=2n(H2SO4)=2×0.1mol/L×0.1L=0.02mol,n(H+):n(NO3- )=0.02mol:0.4mol=
<
,所以氢离子有剩余,根据硝酸根离子计算溶解铜的质量,
设溶解Cu的质量为x,
3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
192g 2mol
x 0.02mol
192g:2mol=x:0.02mol
x=
=1.92g,
故答案为:1.92g.
| ||
| 2 |
| 1 |
| 20 |
| 1 |
| 4 |
设溶解Cu的质量为x,
3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
192g 2mol
x 0.02mol
192g:2mol=x:0.02mol
x=
| 192g×0.02mol |
| 2mol |
故答案为:1.92g.
点评:本题考查根据方程式的计算,明确物质之间的反应是解本题关键,注意进行过量计算,注意转移电子守恒、原子守恒的利用,题目难度中等.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
下列有关物理量相应的单位,表达不正确的是( )
| A、摩尔质量:g?mol-1 |
| B、密度:g?mL-1 |
| C、气体摩尔体积:L |
| D、阿伏加德罗常数:mol-1 |
类推是化学学习中的常用方法,但类推的结论最终要经过实践的检验才能证明其正确与否.下列类推结论中正确的是( )
| A、第Ⅳ族氢化物沸点:CH4<SiH4,则第Ⅴ族氢化物沸点:NH3<PH3 |
| B、第二周期元素氢化物稳定性顺序是HF>H2O>NH3,则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
| C、可电解熔融氯化镁制取金属镁,则也能用电解熔融氯化铝制取金属铝 |
| D、晶体中有阴离子,必有阳离子,则晶体中有阳离子,也必有阴离子 |
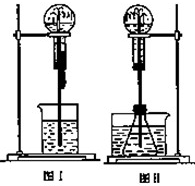 喷泉是一种常见的实验现象(如图),其产生原因是存在压强差.
喷泉是一种常见的实验现象(如图),其产生原因是存在压强差.