题目内容
4.二氧化碳和钠在一定条件下可制得金刚石,其化学方程式为3CO2+4Na=2X+C(金刚石).设NA为阿伏加德罗常数的值,下列有关此反应的叙述不正确的是( )| A. | 金刚石和石墨互为同素异形体 | |
| B. | Na的还原性强于金刚石 | |
| C. | 46g Na完全反应需要标准状况下CO2的体积为33.6L | |
| D. | 当有0.4mo1 Na参与反应时,被还原的CO2的分子数目为0.2NA |
分析 A.同素异形体是同种元素形成的不同单质;
B.氧化还原反应中还原剂的还原性大于还原产物的还原性;
C.根据n=$\frac{m}{M}$计算Na的物质的量,根据方程式计算需要二氧化碳物质的量,再根据V=nVm计算二氧化碳体积;
D.由原子守恒可知X为Na2CO3,被还原的二氧化碳生成碳,根据电子转移守恒计算被还原的二氧化碳物质的量,再根据N=nNA计算被还原的CO2的分子数目.
解答 解:A.金刚石和石墨都是碳的单质,属于同素异形体,故A正确;
B.该反应中Na是还原剂,金刚石是还原产物,则Na的还原性强于金刚石,故B正确;
C.Na的物质的量为$\frac{46g}{23g/mol}$=2mol,根据方程式可知需要二氧化碳物质的量为2mol×$\frac{3}{4}$=1.5mol,标况下二氧化碳体积为1.5mol×22.4L/mol=33.6L,故C正确;
D.由原子守恒可知X为Na2CO3,被还原的二氧化碳生成碳,根据电子转移守恒,被还原的二氧化碳物质的量为$\frac{0.4mol×1}{4}$=0.1mol,则被还原的CO2的分子数目为0.1NA,故D错误,
故选D.
点评 本题考查元素化合物性质、化学方程式计算、氧化还原反应计算等,题目难度中等,侧重于考查学生的分析能力和计算能力,注意把握电子守恒在氧化还原反应计算中的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是( ),添加( )可使该溶液复原.
| A. | NaOH H2O | B. | NaCl H2O | C. | AgNO3 Ag2O | D. | Na2SO4 H2O |
12.已知298K时下述反应的有关数据:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
C(s)+O2 (g)═CO2(g),△H2=-393.5kJ/mol 则 C(s)+CO2(g)=2CO(g) 的△H为( )
C(s)+O2 (g)═CO2(g),△H2=-393.5kJ/mol 则 C(s)+CO2(g)=2CO(g) 的△H为( )
| A. | 283kJ•mol-1 | B. | +172.5 kJ•mol-1 | C. | -172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |
19.下列有关反应限度的叙述正确的是( )
| A. | 可逆反应达到平衡状态后,改变外界条件后,若反应速率发生变化,则平衡一定发生移动 | |
| B. | 大多数化学反应在一定条件下都有一定限度 | |
| C. | 使用催化剂可降低反应活化能,加快反应速率,改变反应限度 | |
| D. | FeCl3溶液与KSCN溶液反应达到平衡时,加入少量KCl溶液,因K+、Cl-一直在溶液中存在,所以溶液颜色不会变化 |
9.下列有关说法不正确的是( )
| A. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 | |
| B. | 将纳米材料(微粒直径是1nm-100nm)分散到分散剂中得到的分散系有丁达尔效应 | |
| C. | 氢氧化铁胶体的制备方法是:将氢氧化铁固体溶于沸水中继续煮沸 | |
| D. | 胶体与其它分散系的本质区别是胶体的分散质粒子的微粒直径在1nm-100nm之间 |
16.下列反应属于加成反应的是( )
| A. | CH4+Cl2 $\stackrel{光}{→}$ CH3Cl+HCl | |
| B. | CH2═CH2+HBr-→CH3CH2Br | |
| C. | CH3COOH+CH3CH2OH$→_{△}^{H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O |
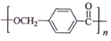 的路线:
的路线: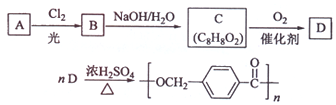
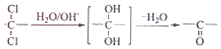
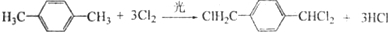 ;
;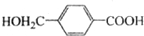 ,由D合成聚酯类高分子材料
,由D合成聚酯类高分子材料 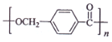 的化学方程式是n
的化学方程式是n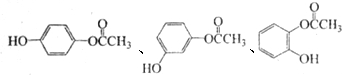 (写结构简式).
(写结构简式).
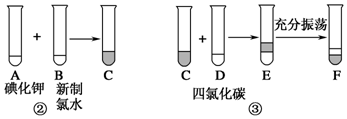
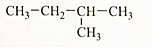
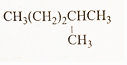 (4)
(4)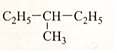 (5)(CH3)2CH-CH2-CH2-CH3.
(5)(CH3)2CH-CH2-CH2-CH3.