题目内容
15.下列各组中的两种气体的分子数一定相同的是( )| A. | 质量相等但密度不等的N2和C2H4 | B. | 体积相同的N2和C2H4 | ||
| C. | 等温、等体积的N2和O2 | D. | 等压、等体积N2和CO2 |
分析 根据N=nNA可知,两种气体的分子数,说明二者的物质的量一定相等,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算出各物质的物质的量,然后进行判断,注意气体摩尔体积的使用条件.
解答 解:根据N=nNA可知,两种气体的分子数,说明二者的物质的量一定相等,
A.N2和C2H4的摩尔质量都是28g/mol,质量相等时二者的物质的量一定相等,则二者一定含有相同的分子数,故A正确;
B.没有指出温度和压强,二者的气体摩尔体积不一定相等,则无法计算N2和C2H4的物质的量,故B错误;
C.没有告诉压强,无法计算N2和O2的物质的量,故C错误;
D.没有指出温度,气体摩尔体积不一定相等,无法计算二者的物质的量,故D错误;
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确气体摩尔体积的使用条件为解答关键,注意熟练掌握物质的量与摩尔质量、阿伏伽德罗常数、气体摩尔体积之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
6.某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到目的是( )
| A. | 将铜丝插入浓硫酸加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色 | |
| B. | 常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成 | |
| C. | 电解CuCl2溶液,若阳极生成11.2L的气体,反应中转移电子为1 mol | |
| D. | 将表面有铜绿的铜器放入盐酸中浸泡,除去铜绿 |
10.下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗涤石油产品中的残余硫酸
②用碳酸氢钠治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
①用氢氧化钠溶液洗涤石油产品中的残余硫酸
②用碳酸氢钠治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
| A. | ①② | B. | ②③④ | C. | ②③ | D. | ①③④ |
20.下列粒子在化学反应中容易得到电子的是( )
| A. | 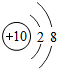 | B. |  | C. | 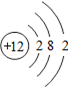 | D. | 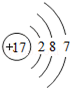 |
7.设NA为阿伏加德罗常数值.下列有关说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 1molN2与4molH2反应生成的NH3分子数为2NA | |
| C. | 1molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 5.6LCO2气体中含有的氧原子数为0.5NA |
1.一包混有杂质的碳酸钠固体,其杂质可能是Ba(NO3)2、KCl及NaHCO3中的一种或两种.今取样品溶于适量水得到澄清溶液.另取10.6克该固体样品跟足量的盐酸反应收集到4.4克二氧化碳,则下列判断中正确的是( )
| A. | 样品中只含一种杂质NaHCO3 | B. | 样品中含有KCl,不含有NaHCO3 | ||
| C. | 样品中含有Ba(NO3)2和NaHCO3 | D. | 样品中含有KCl和NaHCO3 |
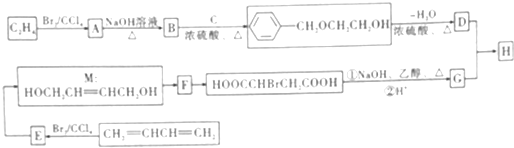
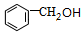 ,F中官能团的名称为羟基、溴原子
,F中官能团的名称为羟基、溴原子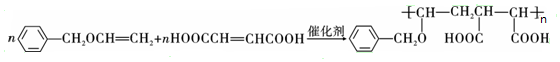
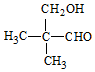 或
或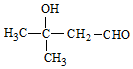 .
.