题目内容
已知以下两个氧化还原反应的化学方程式:
①Cl2+H2O═HCl+HClO ②2Al+Fe2O3
Al2O3+2Fe
(1)表示反应①中的电子转移情况: .
(2)若反应②中每生成56g Fe,转移电子的物质的量是: .
①Cl2+H2O═HCl+HClO ②2Al+Fe2O3
| ||
(1)表示反应①中的电子转移情况:
(2)若反应②中每生成56g Fe,转移电子的物质的量是:
考点:氧化还原反应
专题:推断题
分析:(1)Cl2+H2O═HCl+HClO这,Cl元素的化合价由0降低为-1价,Cl元素的化合价由0升高为+1价,电子转移总数为e-;
(2)n(Fe)=
=1mol,Fe元素的化合价由+3价降低为0,结合化合价计算转移电子.
(2)n(Fe)=
| 56g |
| 56g/mol |
解答:
接:(1)Cl2+H2O═HCl+HClO这,Cl元素的化合价由0降低为-1价,Cl元素的化合价由0升高为+1价,电子转移总数为e-,表示反应①中的电子转移情况为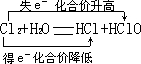 ,
,
故答案为: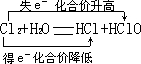 ;
;
(2)根据化学反应②2Al+Fe2O3
Al2O3+2Fe,n(Fe)=
=1mol,Fe元素的化合价由+3价降低为0,转移电子为1mol×(3-0)=3mol,故答案为:3mol.
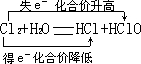 ,
,故答案为:
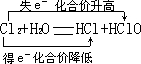 ;
;(2)根据化学反应②2Al+Fe2O3
| ||
| 56g |
| 56g/mol |
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握氧化还原反应中转移的电子数的计算,明确化合价的变化是分析的关键,题目难度不大.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
将Na2O2投入FeCl3溶液中,可观察到的现象是( )
| A、生成白色沉淀 |
| B、生成红褐色沉淀 |
| C、有黄绿色气体产生 |
| D、无变化 |
将一小块金属钠投入到CuSO4溶液中,不可能得到的产物是( )
| A、Cu |
| B、H2 |
| C、Cu(OH)2 |
| D、Na2SO4 |
水溶液中能大量共存的一组离子是( )
| A、Ag+、Ca2+、Cl-、SO42- |
| B、Fe2+、H+、SO32-、ClO- |
| C、Mg2+、NH4+、Cl-、SO42- |
| D、K+、Fe3+、NO3-、SCN- |
下列离子方程式正确的是:
| A、氢氧化铁中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、铝粉溶于氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑ |
| C、在酸性的硫酸亚铁溶液中加入双氧水:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D、硫化氢气体通入氯化铁溶液中:Fe3++H2S=Fe2++S↓+2H+ |
已知反应mx(g)+ny(g)?qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
| A、通入稀有气体使压强增大,平衡向正反应方向移动 |
| B、x的正反应速率是y的逆反应速率的n/m倍 |
| C、降低温度,混合气体的平均相对分子质量变大 |
| D、增加X的物质的量,y的转化率降低 |
 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6