题目内容
对于反应CO2(g)+H2(g)  CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下
CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下
A.加入催化剂,改变了反应的速率,反应的ΔH也随之改变
B.降低温度,反应速率减慢,反应放出的热量不变
C.改变反应体系体积,平衡不发生移动,反应放出的热量不变
D.若将上述反应改为在燃料电池进行,反应放出的热量不变
C
【解析】
试题解析:A、加入催化剂,改变了反应的途径,反应的△H和反应物以及生成物的能量有关,反应的△H不会改变,故A错误;B.降低温度,反应速率减慢,平衡向逆反应方向移动,反应放出的热量变小,度B错误;C、改变反应体系体积即改变压强,对于反应前后气体系数和相等的平衡,不会发生移动,反应放出的热量不变,故C正确;D、在原电池中进行的反应还会伴随电能的转化,并且能量是守恒的,所以反应放出的热量变小,故D错误.
考点:化学平衡

(13分)水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液中,溶液的pH= 。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为 ,由水电离出的c(OH-)= mol·L-1。
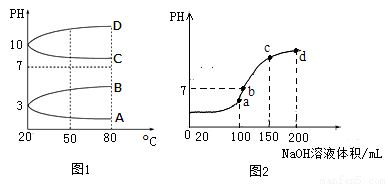
(3)体积均为100 mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,

则HX是 (填“强酸”或“弱酸”),理由是 。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,溶液的pH由大到小的顺序为 (填化学式)。
②25 ℃时,在0.5 mol/L 的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的 倍。
 溶液洗涤并灼烧铂丝后,再进行焰色反应
溶液洗涤并灼烧铂丝后,再进行焰色反应 = ;乙溶液中所含离子的物质的量浓度由大到小的顺序是 。
= ;乙溶液中所含离子的物质的量浓度由大到小的顺序是 。