题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体 析出 |
蛋白质均发生变性 |
| B | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色 沉淀 |
溶液X中不一定含有SO42- |
| C | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色 沉淀 |
H2SiO3的酸性比H2CO3的酸性强 |
| D | 向浓度均为0.1mol?L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色 沉淀 |
Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氯化钠可使蛋白质发生盐析;
B.不能排除SO32-的影响;
C.H2SiO3的酸性比H2CO3的酸性弱;
D.溶度积越小,越易生成沉淀.
B.不能排除SO32-的影响;
C.H2SiO3的酸性比H2CO3的酸性弱;
D.溶度积越小,越易生成沉淀.
解答:
解:A.蛋白质中加入NaCl发生盐析,加入CuSO4发生变性,故A错误;
B.若溶液X中含有SO32-,加入稀HNO3,则会被氧化成SO42-,而与Ba2+生成沉淀,故B正确;
C.反应方程式为:CO2+H2O+Na2SiO3═H2SiO3↓+Na2CO3,该反应发生的原理为强酸制弱酸,即酸性:H2CO3>H2SiO3,故C错误;
D.反应总是向着生成更难溶的物质的方向进行,由于AgI的溶度积比AgCl小,所以优先生成AgI,故D正确.
故选BD.
B.若溶液X中含有SO32-,加入稀HNO3,则会被氧化成SO42-,而与Ba2+生成沉淀,故B正确;
C.反应方程式为:CO2+H2O+Na2SiO3═H2SiO3↓+Na2CO3,该反应发生的原理为强酸制弱酸,即酸性:H2CO3>H2SiO3,故C错误;
D.反应总是向着生成更难溶的物质的方向进行,由于AgI的溶度积比AgCl小,所以优先生成AgI,故D正确.
故选BD.
点评:本题考查较为综合,涉及蛋白质的性质、物质的检验以及难溶电解质的溶解平衡等知识,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握实验操作要点,结合物质的性质综合考虑,难度中等.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
 25℃时,由弱酸(HA)及其盐(NaA)组成的混合溶液,起始浓度均为1mol?L-1.如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入H+或OH-的物质的量而变化的曲线.下列说法中,正确的是( )
25℃时,由弱酸(HA)及其盐(NaA)组成的混合溶液,起始浓度均为1mol?L-1.如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入H+或OH-的物质的量而变化的曲线.下列说法中,正确的是( )| A、加NaOH,HA电离平衡常数增大 |
| B、通入HCl,溶液中阴离子浓度之和减小 |
| C、溶液中水的电离程度a>b>c |
| D、b点溶液中,c(HA)<c(A-) |
设表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| B、常温下,1L O.1mol/L NH4NO3的溶液中含氮原子数为0.2NA |
| C、室温下,21.Og乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
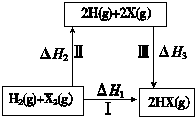 关于如图所示转化关系(X代表卤素),说法不正确的是( )
关于如图所示转化关系(X代表卤素),说法不正确的是( )| A、2H(g)+2X(g)═2HX(g)△H3<0 |
| B、途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 |
| C、Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
| D、途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L SO3中含有的氧原子数为3NA |
| B、标准状况下,22.4L Cl2与足量的稀NaOH 溶液反应,转移电子总数为2NA |
| C、1mol N5+共有34NA核外电子 |
| D、0.5mol CCl4中含有共价键数目为4NA |
以石油为原料可进行如下转化.下列说法正确的是( )
石油→乙烯→乙醇→乙酸→乙酸乙酯.
石油→乙烯→乙醇→乙酸→乙酸乙酯.
| A、石油通过分馏可直接得到乙烯 |
| B、乙烯、聚乙烯的最简式均为CH2,二者互为同分异构体 |
| C、可用氢氧化钠溶液来区别乙醇和乙酸 |
| D、乙醇、乙酸和乙酸乙酯都能发生取代反应 |
化学与人类生产、生活、社会可持续发展密切相关.下列有关说法错误的是( )
| A、煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 |
| B、在汽车排气管上加装“催化转化器”是为了减少有害气体的排放 |
| C、硬铝属于合金材料,瓷器属于硅酸盐制品 |
| D、食醋可去除水垢,NH4Cl溶液可去除铁锈 |