题目内容
X、Y、Z、W是元素周期前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第 周期 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式).
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是 (写化学式,下同),键长较长的是 .
(3)W的基态原子核外电子排布式是 W2Y在空气中煅烧生成W2O的化学方程式是 .
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在
(3)W的基态原子核外电子排布式是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;常温常压下,Y单质是淡黄色固体,常在火山口附近沉积,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;W的一种核素的质量数为63,中子数为34,则其质子数=63-34=29,则W为Cu元素,据此解答.
解答:
解:X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;常温常压下,Y单质是淡黄色固体,常在火山口附近沉积,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;W的一种核素的质量数为63,中子数为34,则其质子数=63-34=29,则W为Cu元素,
(1)Y为硫元素,在周期表中的位置为:第三周期ⅥA族,非金属性Cl>S,故酸性HClO4>H2SO4,故答案为:三;ⅥA;HClO4;
(2)CS2是一种常用的溶剂,结构与CO2类似,所以分子中存在2个σ键,在H-S、H-Cl两种共价键中,Cl元素的电负性更大,对键合电子的吸引力更强,故H-Cl键的极性较强,由于硫原子半径大于氯,所以键长较长的为H-S,
故答案为:2;H-Cl;H-S;
(3)W为Cu元素,质子数为29,原子核外电子数为29,基态原子核外电子排布为1s22s22p63s23p63d104s1,Cu2S在空气中煅烧生成Cu2O的化学方程式是2Cu2S+3O2
2Cu2O+2SO2,
故答案为:1s22s22p63s23p63d104s1;2Cu2S+3O2
2Cu2O+2SO2.
(1)Y为硫元素,在周期表中的位置为:第三周期ⅥA族,非金属性Cl>S,故酸性HClO4>H2SO4,故答案为:三;ⅥA;HClO4;
(2)CS2是一种常用的溶剂,结构与CO2类似,所以分子中存在2个σ键,在H-S、H-Cl两种共价键中,Cl元素的电负性更大,对键合电子的吸引力更强,故H-Cl键的极性较强,由于硫原子半径大于氯,所以键长较长的为H-S,
故答案为:2;H-Cl;H-S;
(3)W为Cu元素,质子数为29,原子核外电子数为29,基态原子核外电子排布为1s22s22p63s23p63d104s1,Cu2S在空气中煅烧生成Cu2O的化学方程式是2Cu2S+3O2
| ||
故答案为:1s22s22p63s23p63d104s1;2Cu2S+3O2
| ||
点评:本题考查了元素周期表、元素周期律、核外电子排布规律、氧化还原反应等,难度不大,推断元素是解题关键,注意基础知识的全面掌握.

练习册系列答案
相关题目
X、Y、Z、M、W原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,Z与其同主族的短周期无素可形成一种常见气体,X、Y、Z3种元素形成化合物甲,下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、化合物甲中可能含有离子键和共价键 |
| C、由W元素形成的单质在自然界的贮量丰富,并存在大量的单质 |
| D、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM |
某同学用Na2CO3配制0.10mol/L Na2CO3溶液的过程如图所示.你认为该同学的错误有( )
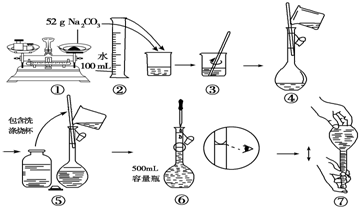

| A、①⑤⑥ | B、②④⑦ |
| C、①⑥ | D、⑤⑥⑦ |
钬的一种同位素
Ho可用于制作医疗激光器,其原子核内中子数与核外电子数之差是( )
165 67 |
| A、31 | B、67 | C、98 | D、165 |
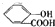 )中液加NaHCO3溶液
)中液加NaHCO3溶液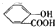 +2HCO3-═
+2HCO3-═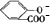 +2CO2↑+2H2O,
+2CO2↑+2H2O,