题目内容
7.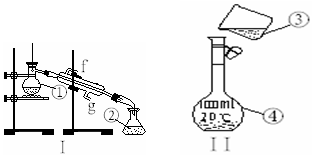 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.(1)写出下列仪器的名称:
①蒸馏烧瓶;②锥形瓶;④容量瓶;
(2)仪器①~④中,使用时必须检查是否漏水的有④;图I实验过程中使用冷凝管时应从g处进水(均填序号).
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有酒精灯;将仪器补充完整后进行的实验操作的名称为:蒸馏.现需配制500ml 0.2mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是未用玻璃棒引流、未采用500ml容量瓶.
分析 (1)根据仪器的结构特点判断;
(2)有活塞和玻璃塞的仪器使用时必须检查是否漏水;冷凝管是下管进水上管出水,冷凝效果好;
(3)四氯化碳和酒精的沸点不同用蒸馏分离;移液时要用玻璃棒,配制溶液时需选择一定的规格的容量瓶.
解答 解:(1)带有支管的烧瓶为蒸馏烧瓶,承接蒸馏产品的是锥形瓶,配制一定物质的量浓度溶液的仪器是容量瓶,
故答案为:蒸馏烧瓶,锥形瓶,容量瓶;
(2)容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水;冷凝管是下管进水上管出水,这样冷却充分,冷凝效果好,
故答案为:④;g;
(3)分离四氯化碳和酒精的混合物,根据沸点不同分离,即用蒸馏的方法,蒸馏需要加热,还需酒精灯;配制一定物质的量浓度的溶液时必须用玻璃棒引流,防止液体外溅,容量瓶只有一个刻度线,只能用来配制所标容量规格的溶液,现需配制500mL只能选用500ml容量瓶,
故答案为:酒精灯;蒸馏;未用玻璃棒引流,未采用500ml容量瓶.
点评 本题考查常见仪器的使用和化学基本操作的方法,题目难度不大,注意在学习中加强基础知识的积累.

练习册系列答案
相关题目
17.恒温下,在容积为2L的甲、乙两个恒容密闭容器中分别充入H2和I2发生可逆反应:
I2(g)+H2(g)═2HI(g)△H=-QkJ•mol-1,实验时有关数据如表:
下列判断正确的是( )
I2(g)+H2(g)═2HI(g)△H=-QkJ•mol-1,实验时有关数据如表:
| 容器编号 | 起始物质的量/mol | 4分钟后平衡时的物质的量/mol | 平衡时放出的热量/kJ | |
| I2 | H2 | HI | ||
| 甲 | 0.01 | 0.01 | 0.004 | Q1 |
| 乙 | 0.02 | 0.02 | a | Q2 |
| A. | 甲容器中,4分钟内氢气的反应速率为5.0×10-4 mol•L-1•min-1 | |
| B. | 平衡时,放出的热量为:Q1=4.0×10-3Q kJ | |
| C. | 平衡后,a=8.0×10-3mol,故乙中HI的质量分数比甲中高 | |
| D. | 该温度下,该反应的平衡常数K=0.25 |
2.下列溶液中Cl-浓度最大的是( )
| A. | 1000mL 2.5mol/L NaCl 溶液 | B. | 300mL 5mol/L KClO3溶液 | ||
| C. | 250mL 1mol/L AlCl3溶液 | D. | 200mL 2mol/L MgCl2 溶液 |
12.下列说法不正确的是( )
| A. | 钠、钾着火时,不能用泡沫灭火器灭火 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| D. | 在汽车尾气系统中装催化转化器,可降低尾气中CO、NOx等的排放量 |
19.下列说法正确的是( )
| A. | 1 mol硫酸与1 mol Ba(OH)2完全中和所放出的热量为中和热 | |
| B. | 101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 | |
| D. | 25℃、101 kPa时,1 mol S和2 mol S的燃烧热相等 |
16.实验室里需用480mL 0.1mol•L-1的硫酸铜溶液,以下说法正确的是( )
| A. | 称取8.0g硫酸铜,加入500mL水 | |
| B. | 称取12.0g胆矾配成500mL溶液 | |
| C. | 定容摇匀后液面下降,应加水至凹液面最低点与刻线相平 | |
| D. | 定容时仰视刻线会使所配溶液浓度偏小 |
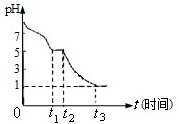 连二亚硫酸钠(Na2S2O4),又称保险粉,是印刷工业中重要的还原剂.某课题小组进行如下实验:
连二亚硫酸钠(Na2S2O4),又称保险粉,是印刷工业中重要的还原剂.某课题小组进行如下实验: