题目内容
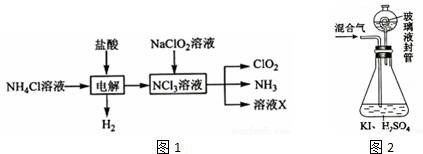
16.高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如图1.
(1)NaOH的电子式是
 .
.(2)检验步骤②反应是否发生的试剂是KSCN.
(3)步骤②反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)从溶液I中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
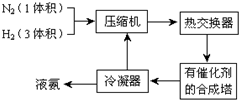
(5)将一定量的Na2FeO4投入到pH不同的污水中(污水中其余成分均相同),溶液中Na2FeO4浓度变化如图2曲线I、II所示,试推测曲线I比曲线II对应的污水pH高(填“高”或“低”).
(6)通过计算得知Na2FeO4的消毒效率(以单位质量得到的电子数表示)比氯气的低(填“高”或“低”),用高铁酸钠代替氯气作净水消毒剂的优点是既能消毒杀菌又能净水(或无毒或方便保存等)(答出两点即可).
分析 氯碱厂电解饱和食盐水生成氯气和氢氧化钠,氯气和氢氧化钠反应生成氯化钠和次氯酸钠,可用结晶的方法除去氯化钠;铁和稀硫酸反应生成硫酸亚铁,加入过氧化氢,生成硫酸铁,次氯酸钠和硫酸铁发生氧化还原反应生成Na2FeO4,以此解答该题,
(1)依据氢氧化钠的化学键的形成过程和电子式书写方法写出电子式;
(2)Fe2+被加过氧化氢氧化为Fe3+,加入检验Fe3+的试剂即可;
(3)依据流程分析判断,步骤②是加入过氧化氢在酸性溶液中氧化亚铁离子为铁离子的过程,依据电子守恒、电荷守恒和原子守恒反应的离子方程式;
(4)碱溶液中次氯酸根离子氧化铁离子为高铁酸根离子,反应的离子方程式依据氧化还原反应电子守恒和原子守恒配平得到;
(5)依据高铁酸根离子发生的还原反应分析判断;
(6)依据高铁酸钠和氯气得到电子转化关系计算分析,根据高铁酸钠是强氧化剂,得到电子生成氢氧化铁胶体分析判断.
解答 解:(1)氢氧化钠是两种化合物,由钠离子和氢氧根离子构成,氢氧根中氧原子和氢原子形成共价键,电子式为: ,
,
故答案为:
(2)Fe2+被加过氧化氢氧化为Fe3+的反应为:2Fe2++H2O2+2H+=2Fe3++2H2O.取样滴入KSCN溶液变红,证明有Fe3+的生成,步骤②反应发生了,
故答案为:KSCN;
(3)步骤②是加入过氧化氢在酸性溶液中氧化亚铁离子为铁离子的过程,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)反应③是碱溶液中次氯酸根离子氧化铁离子为高铁酸根离子,反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(5)依据高铁酸钠在碱性溶液中稳定存在,发生的反应为:FeO42-+3e-+4H2O?Fe(OH)3+5OH-,污水的PH越高平衡逆向进行,PH越小平衡正向进行,依据图象分析Ⅱ先达到平衡需要的时间短,反应速率快,说明污水PH小,曲线I比曲线II对应的污水的PH高;
故答案为:高;
(6)FeO42-+3e-+4H2O?Fe(OH)3+5OH-,单位质量得到电子$\frac{3}{166}$=0.018
Cl2+2e-=2Cl-,单位质量得到电子$\frac{2}{71}$=0.028,所以Na2FeO4的消毒效率比氯气低,高铁酸钠代替氯气作净水消毒剂,利用氧化性起到杀菌消毒作用,利用生成的氢氧化铁胶体起到净水作用;
故答案为:低;既能消毒杀菌又能净水(或无毒或方便保存等).
点评 本题考查了物质制备实验流程的分析判断,主要是物质性质,题干信息的应用,离子方程式的书写是解题关键,题目难度中等.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案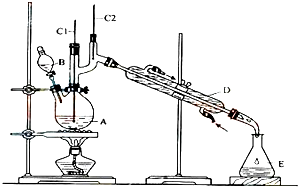 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}加热}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0g.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由不能,浓H2SO4遇水放出大量的热,容易溅出伤人.
(2)加入沸石的作用是防暴沸.若加热后发现未加沸石,应采取的正确方法是停止加热,冷却后补加.
(3)上述装置图中,B的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)B仪器使用前必须进行的操作是C.
a.润湿b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分液时,正丁醛在上层(填“上”或“下”)
(6)反应温度应保持在90-95℃,其原因是既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化,为更好的控制温度,可以采取的改进措施是水浴加热.
(7)本实验中,正丁醛的产率为51%.
| A. | 加入少量W,逆反应速率增大 | |
| B. | 因正反应吸热,所以升高温度正反应速率加快,逆反应速率减慢 | |
| C. | 当v(X)=v(Z)时,反应达到平衡 | |
| D. | 混合气体的密度不变时,反应达到平衡 |
| A. | 减少 | B. | 增大 | ||
| C. | 不变 | D. | 无法判断变化情况 |