题目内容
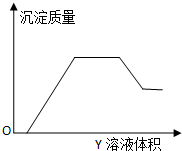 向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,表中符合图象的一组是( )
向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,表中符合图象的一组是( )| X | Y | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A、A | B、B | C、C | D、D |
考点:镁、铝的重要化合物,钠的重要化合物
专题:元素及其化合物
分析:从图中横坐标可以看出,开始加入L的氢氧化钠溶液时,没有产生沉淀,此段是酸与氢氧化钠发生中和反应;
当氢氧化钠继续加入时,沉淀不断增加,直到沉淀最大值;
继续添加氢氧化钠,则沉淀量先不变后又溶解部分,说明沉淀肯定含氢氧化铝和至少一种其他的沉淀,但在于氢氧化铝反应之前,肯定还含有能与氢氧化钠反应但不产生沉淀的物质,据此加以分析;
当氢氧化钠继续加入时,沉淀不断增加,直到沉淀最大值;
继续添加氢氧化钠,则沉淀量先不变后又溶解部分,说明沉淀肯定含氢氧化铝和至少一种其他的沉淀,但在于氢氧化铝反应之前,肯定还含有能与氢氧化钠反应但不产生沉淀的物质,据此加以分析;
解答:
解:A、中间一段沉淀不变的图象没有,故A错误;
B、不会产生沉淀部分溶解的图象,故B错误;
C、低第一段是与盐酸反应,第二段与Al(NO3)3、Fe(NO3)3产生2种沉淀,第三段与NH4NO3反应,第四段是溶解氢氧化铝,故C正确;
D、最终沉淀会全部溶解,故D错误;
B、不会产生沉淀部分溶解的图象,故B错误;
C、低第一段是与盐酸反应,第二段与Al(NO3)3、Fe(NO3)3产生2种沉淀,第三段与NH4NO3反应,第四段是溶解氢氧化铝,故C正确;
D、最终沉淀会全部溶解,故D错误;
点评:本题侧重考查铝及其金属的性质,侧重于学生借助图象分析能力的考查,注意金属及其化合物是重要的无机物,是历年高考的重点,学生在备考过程中应注意积累各物质的性质及重要的化学反应.

练习册系列答案
相关题目
下列说法正确的是( )
| A、向Al2(SO4)3溶液中加过量的NaOH溶液可制备Al(OH)3 |
| B、将过量的过氧化钠投入FeCl2溶液中,最终看到白色沉淀 |
| C、用稀硫酸清洗做焰色反应的铁丝 |
| D、镁合金的硬度和强度均高于纯镁 |
铁铝矾[Al2Fe(SO4)4?XH2O]有净水作用,将其溶于水中得到浅绿色溶液,有关溶液的叙述正确的是( )
| A、该溶液呈中性 |
| B、该溶液中:2c(Al3+)+c(Fe2+)+c(H+)=4c(SO42-)+c(OH-) |
| C、在空气中蒸干并灼烧该溶液,最后所得残留固体为氧化铝和氧化铁 |
| D、向该溶液中加入氢氧化钡溶液,当SO42-完全沉淀是,Al3+、Fe2+恰好被完全沉淀 |
Al2O3
AlCl3
Al(OH)3在以Al2O3为原料制备Al(OH)3时,X适宜用的试剂是( )
| HCl |
| X |
| A、NH3?H2O |
| B、CO2 |
| C、NaOH |
| D、HCl |
在一定条件下,可逆反应X(g)+3Y(g)?2Z(g)达到平衡时,测得Y的转化率为37.5%,X的转化率为25%,则反应开始时,充入容器中的X、Y的物质的量之比是( )
| A、1:3 | B、3:1 |
| C、3:2 | D、1:2 |
下列仪器常用于物质分离的是( )
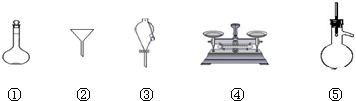

| A、①④⑤ | B、②④⑤ |
| C、②③⑤ | D、①③⑤ |
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法不正确的是( )
| ||
| A、CO2是氧化产物 |
| B、H2C2O4在反应中被氧化 |
| C、1mol H2C2O4参加反应,转移的电子为1mol |
| D、H2C2O4的氧化性强于ClO2的氧化性 |