题目内容
5.将一定量的固体Ag2SO4置于容积不变的密闭容器中(装有少量V2O5),某温度下发生反应:Ag2SO4(s)?Ag2O(s)+SO3(g),2SO3(g)?2SO2(g)+O2(g).反应经过10min后,测得c(SO3)=0.4mol•L-1,c(SO2)=0.1mol•L-1,则下列叙述中不正确的是( )
| A. | 容器里气体的密度为40g•L-1 | |
| B. | SO3的分解率为20% | |
| C. | 化学反应速率v(Ag2SO4)=v(SO3) | |
| D. | 在这10min内的平均反应速率为v(O2)=0.005mol•L-1•min-1 |
分析 已知①Ag2SO4(s)?Ag2O(s)+SO3(g),②2SO3(g)?2SO2(g)+O2(g),经10分钟反应达到平衡,此时c(SO3)=0.4mol/L,c(O2)=0.05mol/L,由反应②可知消耗SO30.1mol/L,生成c (SO2)=0.1mol/L,可知反应①共生成SO3的浓度为0.4mol/L+0.1mol/L=0.5mol/L,以此解答该题.
解答 解:已知①Ag2SO4(s)?Ag2O(s)+SO3(g),②2SO3(g)?2SO2(g)+O2(g),经10分钟反应达到平衡,此时c(SO3)=0.4mol/L,c(O2)=0.05mol/L,由反应②可知消耗SO30.1mol/L,生成c (SO2)=0.1mol/L,可知反应①共生成SO3的浓度为0.4mol/L+0.1mol/L=0.5mol/L,
A.平衡时c (SO2)=0.1mol/L,c (O2)=0.05mol/L,c(SO3)=0.4mol/L,设容器体积为1L,
则m(SO2)=0.1mol/L×1L×64g/mol=6.4g,m(O2)=0.05mol/L×1L×32g/mol=1.6g,m(SO3)=0.4mol/L×1L×80g/mol=32g,则容器内气体密度=$\frac{6.4g+1.6g+32g}{1L}$=40g/L,故A正确;
B.SO3的分解率=$\frac{0.1mol/L}{0.5mol/L}$×100%=20%,故B正确;
C.因为纯固体不可以用来表示反应速率,所以υ(Ag2SO4)表达错误,故C错误;
D.在这10 min内的SO3平均速率=$\frac{0.1mol/L}{10min}$=0.01 mol•L-1•min-1,则氧气表示的反应速率=$\frac{1}{2}$×0.01 mol•L-1•min-1=0.005mol•L-1•min-1,故D正确;
故选C.
点评 本题考查化学平衡计算,为高频考点,侧重考查学生分析计算能力,明确三氧化硫在①②方程式中发生的反应是解本题关键,易错选项是C,注意化学平衡常数表达式和含义,题目难度中等.

 通城学典默写能手系列答案
通城学典默写能手系列答案| A. | Fe2+、Na+、NO3-、Cl- | B. | Mg2+、NH4+、SO42-、NO3- | ||
| C. | H+、K+、Cl-、CH3COO- | D. | K+、Mg2+、CO32-、OH- |
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol,则含0.5 mol NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.65kJ | |
| C. | 可燃物的系数为1的燃烧反应的焓变即为该可燃物的燃烧热 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H=a kJ/mol,2C(s)+O2(g)═2CO(g)△H=b kJ/mol,则a>b |
| A. | Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3- | |
| B. | 用高锰酸钾溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O | |
| C. | 稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| D. | 向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
| A. | 在标准状况下,22.4LCCl4中含5 NA个原子 | |
| B. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1 NA | |
| C. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1 NA | |
| D. | 将100mL0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA |

 .
. 两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯. +H2O
+H2O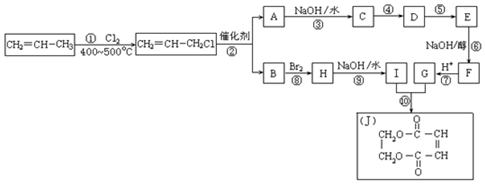
 .
.