题目内容
为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下的密闭容器中,充入一定量的H2和CO,发生反应:2H2(g)+CO(g)
CH3OH(g),测定的部分实验数据如下:
(1)在500s内用H2表示的化学反应速率是 .
(2)在1 000s内用CO表示的化学反应速率是 ,1 000s时CO的转化率是 .
(3)在500s时生成的甲醇的浓度是 .
| ||
| t/s | 0 | 500 | 1 000 |
| c(H2)/(mol?L-1) | 5.00 | 3.52 | 2.48 |
| c (CO)/(mol?L-1) | 2.50 | |
(2)在1 000s内用CO表示的化学反应速率是
(3)在500s时生成的甲醇的浓度是
考点:化学平衡的调控作用
专题:化学平衡专题
分析:据化学方程式求算500s和1000s时CO的浓度;
(1)根据表中数据及v=
计算出在500s内用H2表示的化学反应速率;
(2)根据反应速率表达式v=
计算出1000s内用氢气表示的化学反应速率,然后根据化学计量数与反应速率成正比计算出氢气的反应速率;根据反应速率计算出氢气的转化率;
(3)根据氢气的反应速率计算出消耗氢气的物质的量,再计算出在500s时生成的甲醇的浓度.
(1)根据表中数据及v=
| △c |
| △t |
(2)根据反应速率表达式v=
| △c |
| △t |
(3)根据氢气的反应速率计算出消耗氢气的物质的量,再计算出在500s时生成的甲醇的浓度.
解答:
解:据化学方程式中的化学计量数之比等于反应速率之比,求算出CO在500s时的浓度为
=1.76,1000s时的浓度为
=1.24,故答案为:1.76;1.24;
(1)在500s内用H2表示的化学反应速率为:v(H2)=
=2.96×10-3mol/(L?s),故答案为:2.96×10-3mol/(L?s);
(2)在1000s内用氢气表示的化学反应速率是:v(H2)=
=2.52×10-3mol/(L?s),则1000s内用CO表示的化学反应速率为:v(CO)=
v(H2)=1.26×10-3mol/(L?s);1000s时H2的消耗浓度为:△c(H2)=(5.00-2.48)mol/L=2.52mol/L,氢气的转化率为
×100%=50.4%,
故答案为:1.26×10-3mol/(L?s);50.4%;
(3)在500s时氢气的浓度变化为:△c(H2)=(5.00-3.52)mol/L=1.48mol/L,由反应2H2(g)+CO(g)?CH3OH(g)可知,生成甲醇的物质的量浓度为:c(CH3OH)=
△c(H2)=0.74mol/L,故答案为:0.74mol/L.
| 3.52 |
| 2 |
| 2.48 |
| 2 |
(1)在500s内用H2表示的化学反应速率为:v(H2)=
| (5.00-3.52)mol/L |
| 500s |
(2)在1000s内用氢气表示的化学反应速率是:v(H2)=
| (5.00-2.48)mol/L |
| 1000s |
| 1 |
| 2 |
| 2.52mol/L |
| 5.00mol/L |
故答案为:1.26×10-3mol/(L?s);50.4%;
(3)在500s时氢气的浓度变化为:△c(H2)=(5.00-3.52)mol/L=1.48mol/L,由反应2H2(g)+CO(g)?CH3OH(g)可知,生成甲醇的物质的量浓度为:c(CH3OH)=
| 1 |
| 2 |
点评:本题考查了反应速率的计算,题目难度中等,注意明确化学反应速率与化学计量数成正比,掌握化学反应速率的概念及其表达式.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
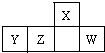 短周期元素X、Y、Z、W在周期表中的相对位置如图,W原子的最外层电子数是其最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在周期表中的相对位置如图,W原子的最外层电子数是其最内层电子数的3倍.下列判断正确的是( )| A、原子半径:X>Y>Z>W |
| B、Y、Z是金属元素 |
| C、最简单气态氢化物的热稳定性:Z>W |
| D、X的氢化物能与其最高价氧化物对应的水化物反应生成盐 |
H2SO4和HNO3的浓度分别为4mol/L和2mol/L的混合液,取10mL加入过量的铁粉,若HNO3的还原产物为NO,则生成气体在标况下的总体积为( )
| A、0.224L |
| B、0.672L |
| C、0.112L |
| D、0.336L |
下列说法中正确的是( )
| A、0.1mol/L (NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B、pH=4的醋酸稀释l0倍,溶液中c(CH3COOH)、c(OH-)均减小 |
| C、常温下向CH3COONa溶液中加入适量CH3COOH溶液,使混合液的pH=7,则混合液中c(Na+)=c(CH3COO-) |
| D、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 |
一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入350mL 2mol?L-1的稀硝酸恰好使混合物完全溶解,放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现.若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
| A、0.21 mol |
| B、0.25 mol |
| C、0.3 mol |
| D、0.35 mol |
下列生活中的化学事例对应的离子方程式书写正确的是( )
| A、用醋酸除去暖瓶中的水垢:2H++CaCO3═Ca2++CO2↑+H2O |
| B、利用Na2CO3溶液可除油污:CO32-+2H2O?H2CO3+2OH- |
| C、氢氧燃料电池在酸性介质中的正极反应:O2+4e-+2H2O=4OH- |
| D、汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
下列各组物质中,都是强电解质的是( )
| A、NaOH、Ca(OH)2、NH3?H2O |
| B、NH4Cl、CH3COOH、Na2S |
| C、HBr、HCl、BaSO4 |
| D、HClO、NaF、Ba(OH)2 |
 低碳经济呼唤新能源和清洁环保能源.煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题.
低碳经济呼唤新能源和清洁环保能源.煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题.