题目内容
某高一化学探究小组的同学设计实验探究0.5
mol/L NaOH溶液、0.5 mol/L 硫酸溶液、0.2 mol/L Na2CO3溶液两两相互反应的情况.(1)配制0.50 mol/L NaOH溶液
①若实验中大约要使用100 mL NaOH溶液,至少需要称量NaOH固体________g;
②从下图中选择称量NaOH固体所需要的仪器(填字母):________,配制0.50 mol/L NaOH溶液还需要的仪器有________.
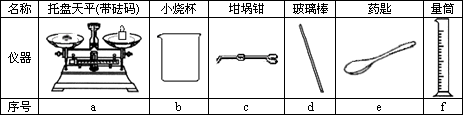
③在配制过程中,下列情况会导致溶液浓度偏高的是________.
A.容量瓶使用前经蒸馏水清洗后没有干燥
B.配制过程中未用蒸馏水洗涤烧杯和玻璃棒
C.俯视确定凹液面与刻度线相切
D.用敞口容器称量NaOH且时间过长
(2)探究相关反应
①将30 mL 0.2 mol/L Na2CO3溶液逐渐加入30 mL 0.5 mol/L H2SO4溶液中,看到的现象是________;
②将2~3滴酚酞溶液滴入60 mL NaOH溶液中,看到的现象是________,向该NaOH溶液中逐渐加入0.5 mol/L H2SO4溶液40 mL,最后所得溶液的溶质为________.
解析:
|
(1)①2.0 ②abe 100 mL容量瓶 ③C (2)①产生气泡 ②溶液变红 Na2SO4和H2SO4 |

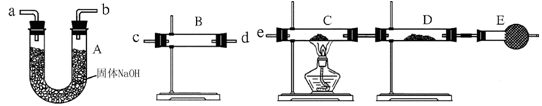
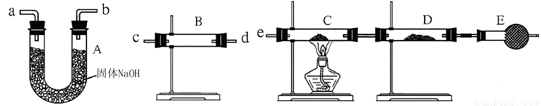
某中学高一化学兴趣小组的同学,在实验室探究用过量的锌与浓硫酸反应制取SO2。
①这样制取的SO2中可能含有的杂质有________。
②某同学用下列装置连接成一整套实验装置以验证①的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是______→______→______→______→______→(用a、b……填写;每套装置只允许使用一次)。

③根据②确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论填入下表:
| 装置 | 所盛药品 | 实验现象 | 结论 |
| B | |||
| C | CuO固体 | ||
| D | 无水CuSO4 |
(9分)
某中学高一化学兴趣小组的同学,在实验室探究用过量的锌与浓硫酸反应制取SO2。
(1)这样制取的SO2中可能含有的杂质有 和 。
(2)某同学用下列装置连接成一整套实验装置以验证①的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是 → → → → → (用a、b……填写;每套装置只允许使用一次)。
(3)根据②确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论填入下表:
| 装置 | 所盛药品 | 实验现象 | 结论 |
| B |
|
|
|
| C | CuO固体 |
|
|
| D | 无水CuSO4 |
|