题目内容
3.已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示: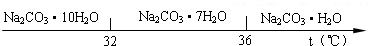
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
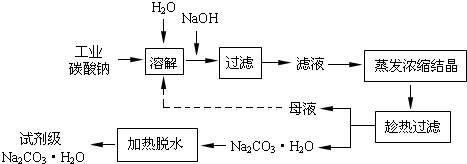
(1)加入NaOH溶液时,反应的离子方程式为Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2↓+CO32-;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021;
(3)“母液”中除了含有Na+、CO32-外,还含有Cl-、SO42-等离子.
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用.请你分析实际工业生产中是否可行不可行(填“可行”或“不可行”),并说明理由若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质;
(5)已知:Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol.
分析 (1)因工业碳酸钠中含有Mg2+,Fe3+,Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3、CaCO3沉淀;
(2)根据氢氧化镁和氢氧化铁的溶解平衡以及溶度积表达式,则当两种沉淀共存且溶液的pH=8时,c(Mg2+)=$\frac{Ksp}{[OH{\;}^{-}]{\;}^{2}}$,(Fe3+)=$\frac{Ksp}{[OH{\;}^{-}]{\;}^{3}}$,据此计算;
(3)除去g2+,Fe3+,Ca2+,滤液中除了含有 Na+、CO32-离子外,还含有Cl-、SO42-;
(4)分析“母液”中存在的离子,若参与循环,将使离子浓度增大,对工业生产中哪个环节有所影响;
(5)已知:①Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1,②Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1,利用盖斯定律,将①-②得到Na2CO3•H2O(S)═Na2CO3(s)+H2O(g),据此书写热化学方程式.
解答 解:(1)碳酸钠中含有Mg2+,Fe3+,Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3、CaCO3沉淀,滤渣的主要成分为Mg(OH)2、Fe(OH)3、CaCO3,发生的发应有:Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg (OH) 2↓+CO32-,
故答案为:Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2↓+CO32-;
(2)根据氢氧化镁和氢氧化铁的溶解平衡以及溶度积表达式,则当两种沉淀共存且溶液的pH=8时,c(Mg2+)=$\frac{Ksp}{[OH{\;}^{-}]{\;}^{2}}$=$\frac{5.61×10{\;}^{-12}}{10{\;}^{-12}}$=5.61mol/L,c(Fe3+)=$\frac{Ksp}{[OH{\;}^{-}]{\;}^{3}}$=$\frac{2.64×10{\;}^{-39}}{10{\;}^{-18}}$=2.64×10-21mol/L,
所以 c(Mg2+):c(Fe3+)=5.61:2.64×10-21=2.125×1021,
故答案为:2.125×1021;
(3)碳酸钠中含有Mg2+,Fe3+,Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3、CaCO3沉淀,过滤后滤液中除了含有 Na+、CO32-离子外,还含有Cl-、SO42-,
故答案为:Cl-、SO42-;
(4)若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质,这样不符合该提纯工艺,
故答案为:不可行;若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质;
(5)已知:①Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1,②Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1,利用盖斯定律,将①-②得到Na2CO3•H2O(S)═Na2CO3(s)+H2O(g),即Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol,
故答案为:Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol.
点评 本题考查了物质的分离、提纯及物质的制取等知识,题目难度中等,本题是一道比较综合的试题题,有利于考查学生分析和解决问题的能力.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案| A. | 量筒、酸式滴定管、水 | B. | 容量瓶、碱式滴定管、苯 | ||
| C. | 量筒、碱式滴定管、水 | D. | 容量瓶、酸式滴定管、四氯化碳 |
(1)向FeBr2溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是Fe3+,用实验证明你的观点,简述实验操作及现象取适量反应后的溶液滴加KSCN溶液变红.
(2)己知常温下一些电解质的相关数据见下表:
| H2CO3 | K${\;}_{{a}_{1}}$=4.3×10-7 | HClO | Ka=2.95×10-8 |
| K${\;}_{{a}_{2}}$=5.61×10-11 | AgCl | Ksp=1.77×10-10 | |
| CH3COOH | Ka=1.76×10-5 | Ag2CrO4 | Ksp=1.12×10-12 |
②向浓度均为0.010mol/L的NaCl,Na2Cr04组成的混合溶液中逐滴加入浓度为0.010mol•L-1AgN03溶液,首先生成的沉淀其化学式为AgCl.
(3)分别向四份各100mL,浓度均为2mo1L-1的FeC13溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
| I | Ⅱ | Ⅲ | Ⅳ | |
| FeCl3溶液体积/mL | 100 | 100 | 100 | 100 |
| 加入粉末质量/g | 3 | 6.6 | 9 | 12 |
| 剩余粉末质量/g | 0 | 0.64 | 3.2 | 6.4 |
②根据表中的数据分析I反应后的溶液中存在的金属阳离子有〔用离子符号表示)Fe3+、Fe2+、Cu2+.
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | HCO3-的电离方程式:HCO3-+H2O═H2CO3+OH- | |
| D. | Cl2与H2O反应:Cl2+H2O═H++Cl-+HClO |
| A. | 铁 | B. | 碳 | C. | 铜 | D. | 铝 |
| A. | V(A)=0.15mol/(l•s) | B. | V(B)=0.6mol/(l•s) | C. | V(C)=0.45mol/(l•s) | D. | V(D)=4.0mol/(l•min) |
 如图表示A--E 五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.
如图表示A--E 五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.