题目内容
7.下列有关分子、原子、离子说法正确的是( )| A. | 分子是化学变化中最小的粒子 | |
| B. | 一切原子的原子核都是由质子、中子构成的 | |
| C. | 分子的质量总比原子质量大 | |
| D. | 分子、原子、离子都能直接构成物质 |
分析 A、从原子是化学变化中的最小粒子,分子在化学变化中可以再分去分析;
B、氢原子的一种同位素氕不含中子;
C、从分子的质量不一定比原子的质量大,如水分子的质量比铁原子的质量小去分析;
D、从分子、原子、离子都能直接构成物质去分析.
解答 解:A、原子是化学变化中的最小粒子,分子在化学变化中可以再分,故A错误;
B、氢原子的一种同位素氕原子不含中子,故B错误;
C、分子的质量不一定比原子的质量大,如水分子的质量比铁原子的质量小,故C错误;
D、分子、原子、离子都能直接构成物质,故D正确;
故选D.
点评 本题难度不大,掌握分子、原子、离子的结构和性质是解决本题的关键,掌握基础是解题关键.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
6.下列说法正确的是( )

| A. | 金属发生吸氧腐蚀时,被腐蚀的速率和氧气浓度无关 | |
| B. | 标准状况下,2.24LCCl4分子中共价键的数目为0.4×6.02×1023 | |
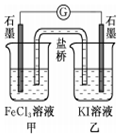
| C. | 控制适合的条件,将反应2Fe3++2I-═2Fe2++I2设计成如图所示的原电池.当电流汁读数为零后,在甲中溶入FeCl2固体,则乙中石墨电极为负极 | |
| D. | 向盛有2mL饱和H2S溶液的两支试管中分别滴加1滴浓度均为0.1mol/L的ZnSO4溶液和CuSO4溶液,有CuS生成而无ZnS生成,则Ksp(CuS)<Ksp(ZnS) |
18.下列除去杂质的操作中不正确的是( )
| A. | CuO中混有Al2O3:加入过量烧碱溶液充分反应后过滤 | |
| B. | FeCl2溶液中混有CuCl2:加入过量铁粉充分反应后过滤 | |
| C. | Na2CO3固体中混有少量NaHCO3:加入过量NaOH溶液,反应后加热蒸干 | |
| D. | 乙烷中混有乙烯:将混合气体通过盛溴水的洗气瓶 |
15.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) $?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| D. | 氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |
2.体积为1L干燥容器中充入HCl气体后,测得容器中气体对氧气的相对密度为1.082(空气的平均摩尔质量为29g/mol).则容器中HCl气体的体积为( )
| A. | 0.25L | B. | 0.5L | C. | 0.75L | D. | 1L |
19.下列说法正确的是( )
| A. | 6.02×1023就是阿伏加德罗常数 | |
| B. | 1mol氧含 6.02×1023个 O2 | |
| C. | 1mol任何气体所含的气体分子数目都相等 | |
| D. | 摩尔是国际单位制中的一个基本物理量 |
16.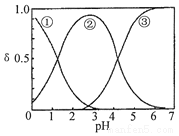 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )| A. | 曲线①代表的粒子是HC2O4- | |
| B. | 0.1mol•L-1NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)增大 |
4.下列说法错误的是( )
| A. | 焰色反应与电子跃迁有关 | |
| B. | P4和CH4都是正四面体分子且键角都为109°28′ | |
| C. | 元素电负性越大的原子,吸引电子的能力越强 | |
| D. | 根据对角线规则,H3BO3是弱酸 |