题目内容
次磷酸(H3PO2)可发生下列反应而用于化学镀银。
Ag++ H3PO2+ H2O — Ag + H3PO4+ H+
试回答下列问题:
H3PO2中,P元素的化合价为________;该反应中,H3PO2做 (氧化剂、还原剂)
H3PO2是一种中强酸,写出其电离方程式: 。
配平离子方程式。
用双线桥法标出电子转移的数目。
若反应中生成5.4 g Ag,则转移电子个数为 。
已知重水(D2O)和乙酸之间会发生氢交换:
D2O+CH3COOH CH3COOD+HDO
CH3COOD+HDO
次磷酸(H3PO2)与D2O之间也能发生氢交换,但次磷酸钠(NaH2PO2)与D2O之间不能发生氢交换,从分类来看,NaH2PO2属于
A.正盐 B.酸式盐 C.钠盐 D.氧化物
(1)+1 还原剂 (2)H3PO2 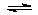 H+ + H2PO2-
H+ + H2PO2-
(3)配平离子方程式。(未写“=”扣1分)
(4)用双线桥法在上式中标出电子转移的数目。

(5)0.05NA(答3.01×1022此处视为准确) (6)AC
【解析】
试题分析:(1)据化合价代数和为0可知P化合价为+1价,P化合价由+1价+5价,故H3PO2作还原剂;
(2)H3PO2属于中强酸,不能完全电离,用可逆符号;
(3)据原子个数守恒和得失电子总数守恒可知,配平的系数为4、1、2、4、14;
(4)双线桥,从失电子的元素指向得电子的元素
(5)银生成银离子,失去1个电子,5.4 g Ag物质的量为0.05mol即转移的电子数为3.01×1022;
(6)NaH2PO2属于正盐 、钠盐。
考点:考查氧化还原反应的相关知识点。

 小学教材完全解读系列答案
小学教材完全解读系列答案
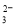
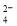
 A.由图1所示曲线可知,化学催化比酶催化的效果好
A.由图1所示曲线可知,化学催化比酶催化的效果好 2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率