题目内容
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属,溶液F中加入NaOH 溶液出现白色沉淀,该白色沉淀会迅速转化成灰绿色,最后变成红褐色沉淀.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出).
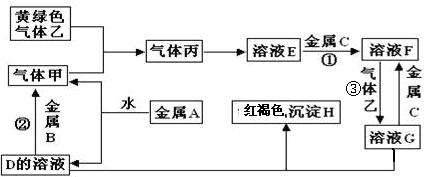
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A ;H ; 乙 .
(2)写出下列反应的离子方程式:)金属A与水反应 反应② 反应③
(3)金属C可以与水蒸气在高温下反应,生成 (填化学式)和氢气.

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应的离子方程式:)金属A与水反应
(3)金属C可以与水蒸气在高温下反应,生成
考点:无机物的推断
专题:
分析:有三种金属单质A、B、C,其中A的焰色反应为黄色,所以A一定是金属钠,钠和水反应生成氢气和氢氧化钠,甲是氢气,D的溶液是氢氧化钠,气体乙为黄绿色,故乙为氯气,气体丙是氯化氢,所以E是盐酸,红褐色的沉淀H是氢氧化铁,所以金属C是铁,F是氯化亚铁,能和氢氧化钠反应生成氢气的金属只有铝,所以B是铝.
解答:
解:有三种金属单质A、B、C,其中A的焰色反应为黄色,所以A一定是金属钠,钠和水反应生成氢气和氢氧化钠,甲是氢气,D的溶液是氢氧化钠,气体乙为黄绿色,故乙为氯气,气体丙是氯化氢,所以E是盐酸,红褐色的沉淀H是氢氧化铁,所以金属C是铁,F是氯化亚铁,能和氢氧化钠反应生成氢气的金属只有铝,所以B是铝,
(1)由上分析知A为Na,H为Fe(OH)3,乙为Cl2,故答案为:Na;Fe(OH)3;Cl2;
(2)金属A与水反应方程式为2Na+2H2O═2NaOH+H2↑,反应②为铝与氢氧化钠反应,方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,反应③为氯气与氯化亚铁反应,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Na+2H2O═2NaOH+H2↑;2Al+2OH-+2H2O═2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)金属Fe可以与水蒸气在高温下反应,产物为Fe3O4,故答案为:Fe3O4.
(1)由上分析知A为Na,H为Fe(OH)3,乙为Cl2,故答案为:Na;Fe(OH)3;Cl2;
(2)金属A与水反应方程式为2Na+2H2O═2NaOH+H2↑,反应②为铝与氢氧化钠反应,方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,反应③为氯气与氯化亚铁反应,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Na+2H2O═2NaOH+H2↑;2Al+2OH-+2H2O═2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)金属Fe可以与水蒸气在高温下反应,产物为Fe3O4,故答案为:Fe3O4.
点评:此题主要考查学生的综合分析能力,要求同学们具备有关物质的基础知识,解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有机物:①甲酸乙酯;②乙酸;③乙酸乙酯;④丙醛;⑤乙醇; ⑥葡萄糖中,能发生银镜反应的是( )
| A、①②③ | B、①③④ |
| C、②⑤⑥ | D、①④⑥ |
比较等物质的量浓度的:①H2SO3;②NaHSO3;③Na2SO3.三种溶液中c(SO32-)浓度的大小,排列正确的是( )
| A、①>②>③ |
| B、③>②>① |
| C、②>①>③ |
| D、③>①>② |
下到实验不能证明HR为弱酸的是( )
| A、室温下,NaR溶液的pH大于7 |
| B、加热NaR溶液时,溶液的pH变小 |
| C、将锌粒分别投入到1 mol?L-1的盐酸和HR中,HR产生氢气的速率慢 |
| D、室温下,0.1 mol?L-1HR的pH>1 |
下列水解的离子方程式正确的是( )
| A、HS-+H2O?S2++H2O+ |
| B、Fe3++3H2O?Fe(OH)3↓+3H+ |
| C、CO32-+2H2O?H2CO3+2OH- |
| D、NH4++H2O?NH3?H2O+H+ |
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
| A、Ba(OH)2和Ba(HCO3)2 |
| B、AlCl3和NaOH |
| C、NaAlO2和H2SO4 |
| D、Ba(OH)2和NaHSO4 |
用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应.下列有关叙述不正确的是( )
| A、所消耗的硝酸的量:①>②>③ |
| B、对环境造成的危害,③最小 |
| C、因铜与浓硝酸作用最快,故制取硝酸铜的最佳方案是① |
| D、三种途径所消耗的铜的质量不相等 |
下列离子方程式不正确的是( )
| A、将2mol/L NaAlO2溶液和3mol/L的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
| B、向1mol/L明矾溶液50mL中滴入数滴0.1mol/L Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
| D、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |