题目内容
已知H2O2既具有氧化性,又具有还原性,下列有关H2O2的说法正确的是( )
| A、将足量的H2O2加入H2SO4和KI的混合溶液中产生无色气体,溶液变成棕色,发生的反应可能为:H2O2+2I-═I2+O2↑+2H+ | ||
| B、将H2O2和HBrO溶液混合,产生无色气体,发生的反应可能为:4HBrO+2H2O2═4HBr+3O2↑+2H2O | ||
| C、常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+═2Fe3++2H2O,2Fe3++H2O2═2Fe2++O2↑+2H+,可认为Fe2+能催化H2O2的分解 | ||
D、在酸性条件下,高锰酸钾溶液与双氧水发生反应,其离子方程式为2MnO
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.根据电荷守恒判断,该离子方程式不满足电荷守恒;
B.根据电子守恒判断,该离子方程式中化合价升降不相等;
C.根据催化剂的特点及两个反应中亚铁离子在反应前后的变化进行解答;
D.根据电子守恒判断,该氧化还原反应中化合价变化不相等,违反了电荷守恒.
B.根据电子守恒判断,该离子方程式中化合价升降不相等;
C.根据催化剂的特点及两个反应中亚铁离子在反应前后的变化进行解答;
D.根据电子守恒判断,该氧化还原反应中化合价变化不相等,违反了电荷守恒.
解答:
解:A.将足量的H2O2加入H2SO4和KI的混合溶液中产生无色气体氧气,碘离子被氧化成碘单质,溶液变成棕色,正确的离子方程式为:2H++3H2O2+2I-═I2+O2↑+4H2O,故A错误;
B.将H2O2和HBrO溶液混合,产生无色气体为氧气,HBrO中Br的化合价为+1价,反应后生成-1价的HBr,化合价降低2价,双氧水中-1价氧元素被氧化成0价的氧气,化合价升高1价,1分子双氧水反应化合价升高2价,则双氧水与HBrO的计量数相等,配平后的反应为:HBrO+H2O2═HBr+O2↑+H2O,故B错误;
C.常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+═2Fe3++2H2O,2Fe3++H2O2═2Fe2++O2↑+2H+,两个反应中,亚铁离子反应前后没有发生变化,所以可认为Fe2+能催化H2O2的分解,故C正确;
D.酸性条件下,高锰酸钾溶液与双氧水发生反应,双氧水被氧化成氧气,离子方程式必须满足电子守恒,正确的离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故D错误;
故选C.
B.将H2O2和HBrO溶液混合,产生无色气体为氧气,HBrO中Br的化合价为+1价,反应后生成-1价的HBr,化合价降低2价,双氧水中-1价氧元素被氧化成0价的氧气,化合价升高1价,1分子双氧水反应化合价升高2价,则双氧水与HBrO的计量数相等,配平后的反应为:HBrO+H2O2═HBr+O2↑+H2O,故B错误;
C.常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+═2Fe3++2H2O,2Fe3++H2O2═2Fe2++O2↑+2H+,两个反应中,亚铁离子反应前后没有发生变化,所以可认为Fe2+能催化H2O2的分解,故C正确;
D.酸性条件下,高锰酸钾溶液与双氧水发生反应,双氧水被氧化成氧气,离子方程式必须满足电子守恒,正确的离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
给物质分类时由于标准不同往往会出现( )
| A、树状分类法 |
| B、环状分类法 |
| C、球状分类法 |
| D、交叉分类法 |
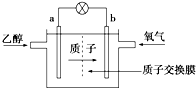 美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子(H+)作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应式为C2H5OH+3O2═2CO2+3H2O,电池示意图如图所示.下列说法不正确的是( )
美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子(H+)作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应式为C2H5OH+3O2═2CO2+3H2O,电池示意图如图所示.下列说法不正确的是( )| A、a为电池的负极 |
| B、b电极发生氧化反应 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:4H++O2+4e-═2H2O |
同周期的三种非金属元素X、Y、Z,它们的原子半径由小到大的顺序是X<Y<Z,则下列判断中,正确的是( )
| A、元素的非金属性:X<Y<Z |
| B、气态氢化物的稳定性按X、Y、Z顺序增强 |
| C、X、Y、Z的最高价氧化物水化物的酸性由强到弱 |
| D、X、Y、Z原子的最外层电子数依次增多 |
下列事实不能用平衡移动原理解释的是( )
| A、将氯化铁溶液加热蒸干最终得不到氯化铁固体 |
| B、钢铁在潮湿的空气中容易生锈 |
| C、温度过高对合成氨不利 |
| D、热的纯碱溶液易去油污 |
如图所示: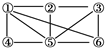 6个编号分别代表下列物质中的一种物质a.Al;b.Fe2O3;c.NaOH溶液;d.氢碘酸溶液;e.NH3;f.O2.凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )
6个编号分别代表下列物质中的一种物质a.Al;b.Fe2O3;c.NaOH溶液;d.氢碘酸溶液;e.NH3;f.O2.凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )
 6个编号分别代表下列物质中的一种物质a.Al;b.Fe2O3;c.NaOH溶液;d.氢碘酸溶液;e.NH3;f.O2.凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )
6个编号分别代表下列物质中的一种物质a.Al;b.Fe2O3;c.NaOH溶液;d.氢碘酸溶液;e.NH3;f.O2.凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )| A、a或b | B、c | C、d | D、e或f |
往FeCl3溶液中滴加少量KSCN溶液,溶液呈红色,发生如下反应: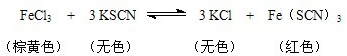
下列说法中正确的是( )
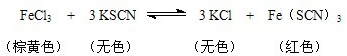
下列说法中正确的是( )
| A、往上述溶液中滴入Fe2(SO4)3溶液,溶液红色变浅 |
| B、往上述溶液中滴入NH4SCN溶液,溶液红色不变 |
| C、往上述溶液中加入铁粉,溶液红色加深 |
| D、往上述溶液中滴入NaOH溶液,溶液红色变浅 |
下列说法正确的是( )
| A、非金属元素之间只能形成共价化合物 |
| B、含有离子键的化合物不一定是离子化合物 |
| C、含有共价键的化合物一定是共价化合物 |
| D、离子化合物中可能含有极性键和非极性键 |