题目内容
11.在一定的温度下,向一个容积为2L的恒容密闭容器中(事先装入催化剂),充入2molN2和3molH2,3min后测得密闭容器内的压强是起始时的0.9倍.在这段时间内,用H2表示该反应的平均反应速率是( )| A. | 0.125mol•L-1•min-1 | B. | 0.100 mol•L-1•s-1 | ||
| C. | 0.200 mol•L-1•min-1 | D. | 0.375 mol•L-1•s-1 |
分析 发生3H2+N2?2NH3,设参加反应的氮气的物质的量为x,则
3H2+N2?2NH3
开始 3 2 0
转化 3x x 2x
3min 3-3x 2-x 2x
3min后测得密闭容器内的压强是起始时的0.9倍,则$\frac{3-3x+2-x+2x}{3+2}$=0.9,
解得x=0.25,
结合v=$\frac{△c}{△t}$计算.
解答 解:发生3H2+N2?2NH3,设参加反应的氮气的物质的量为x,则
3H2+N2?2NH3
开始 3 2 0
转化 3x x 2x
3min 3-3x 2-x 2x
3min后测得密闭容器内的压强是起始时的0.9倍,则$\frac{3-3x+2-x+2x}{3+2}$=0.9,
解得x=0.25,
v(H2)=$\frac{△c}{△t}$=$\frac{\frac{3×0.25mol}{2L}}{3min}$=0.125mol•L-1•min-1.
故选A.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、反应速率的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量比等于压强比,题目难度不大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
1.将0.2mol AgNO3、0.4mol Cu(NO3)2和0.6mol KCl溶于水配成100mL溶液,用惰性电极电解一段时间后,在一极上析出0.3mol Cu,此时,另一极上的气体体积(标准状况)为( )
| A. | 4.48 L | B. | 5.6 L | C. | 6.7 L | D. | 7.8 L |
2.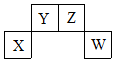 短周期元素X、Y、Z、W在周期表中的位置关系如图,X元素的单质既能与强酸溶液反应,又能与强碱溶液反应.下列说法正确的是( )
短周期元素X、Y、Z、W在周期表中的位置关系如图,X元素的单质既能与强酸溶液反应,又能与强碱溶液反应.下列说法正确的是( )
 短周期元素X、Y、Z、W在周期表中的位置关系如图,X元素的单质既能与强酸溶液反应,又能与强碱溶液反应.下列说法正确的是( )
短周期元素X、Y、Z、W在周期表中的位置关系如图,X元素的单质既能与强酸溶液反应,又能与强碱溶液反应.下列说法正确的是( )| A. | X的单质投入冷浓硫酸中剧烈反应 | |
| B. | 几种最低价气态氢化物稳定性:Z>W | |
| C. | W的氧化物对应的水化物一定是强酸 | |
| D. | Z的氧化物对环境有污染,Y的氧化物没有污染 |
6.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | Na2O2中既含有离子键又含有非极性共价键 | |
| C. | KOH中只含有共价键 | |
| D. | KI和HI中化学键类型完全相同 |
16.下列结论错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 微粒半径:K+>Al3+>S2->Cl- | |
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | |
| D. | 金属性:K>Ca>Mg>Be |
3.可逆反应:2NO2$\stackrel{△}{?}$2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是:①单位时间内生成n molO2的同时生成2n molNO2②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态③混合气体的颜
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ①③⑤⑥ | D. | 全部 |
20.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 | |
| B. | 制作航天服的聚脂纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | 重金属离子能杀死H7N9禽流感病毒 |
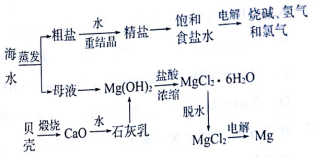
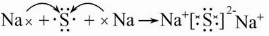 .
.