题目内容
14.对于常温常压下的22.4LSO2,下列有关说法正确的是( )(NA表示阿伏加德罗常数)| A. | 物质的量为1mol | B. | 质量大于64g | ||
| C. | 含S原子数目大于NA | D. | 含O原子的物质的量小于2mol |
分析 常温常压下,气体摩尔体积不是22.4L/mol,气体摩尔体积大于22.4L/mol,依据n=$\frac{V}{{V}_{m}}$计算物质的量判断.
解答 解:A.常温常压下,气体摩尔体积不是22.4L/mol,物质的量不是1mol,故A错误;
B.常温常压下,气体摩尔体积大于22.4L/mol,22.4LSO2物质的量小于1mol,m=nM,质量小于64g,故B错误;
C.常温常压下,气体摩尔体积大于22.4L/mol,依据n=$\frac{V}{{V}_{m}}$计算物质的量可知物质的量小于1mol,含S原子数目小于NA、,故C错误;
D..常温常压下,气体摩尔体积大于22.4L/mol,依据n=$\frac{V}{{V}_{m}}$计算物质的量可知物质的量小于1mol,含O原子的物质的量小于2mol,故D正确;
故选D.
点评 本题考查了气体摩尔体积的应用条件分析,主要是气体摩尔体积和物质的量的计算应用,注意微粒数的计算,题目较简单.

练习册系列答案
相关题目
4.对下列叙述的评价合理的是( )
| 选项 | 叙述 | 评价 |
| A | 乙酸乙酯在H218O中水解,产物乙醇中将含有18O | 错,根据酯的水解规律,产物乙酸中将含有18O同位素,而乙醇则没有 |
| B | 淀粉与20%的硫酸混合液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全 | 错,淀粉水解后未加碱中和至溶液呈碱性 |
| C | 溴乙烷与NaOH溶液共热充分反应后,再加入AgNO3溶液,能观察到浅黄色沉淀 | 对,溴乙烷水解产生了溴离子 |
| D | 可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和葡萄糖溶液 | 错,用新制的Cu(OH)2悬浊液鉴别乙醇溶液和乙酸溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.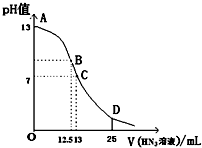 纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )
纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )
 纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )
纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )| A. | 若用已知浓度的NaOH溶液滴定HN3溶液来测定HN3的浓度时应用甲基橙作指示剂 | |
| B. | 常温下,向0.2mol•L-1HN3的溶液中加水稀释,则 $\frac{c({{N}_{3}}^{-})}{c(O{H}^{-})•c(H{N}_{3})}$不变 | |
| C. | 分别中和PH均为4的HN3溶液和HCl溶液,消耗0.1mol•L-1NaOH溶液的体积相同 | |
| D. | D点时溶液中离子浓度存在如下关系:c(H+)+c(HN3)=c(N3-)+c(OH-) |
9.化学是以实验为基础的科学,下列有关实验现象描述不正确的是( )
| 选项 | 实验操作 | 实验现象 |
| A | 在氧气中点燃Mg条 | 发出耀眼白光,生成白色固体 |
| B | 将乙烯通入酸性高锰酸钾溶液 | 溶液褪色 |
| C | 将点燃的Na块伸入Cl2瓶中 | Na块剧烈燃烧,生成大量黑烟 |
| D | 将碘水滴到新切的土豆片上 | 土豆片表面变蓝 |
| A. | A | B. | B | C. | C | D. | D |
1. 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.(已知:S2O32-+2H+═H2O+S↓+SO2↑)
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(3)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.
(已知 I2+2S2O32-═S4O62-+2I-,其中Na2S2O3溶液均足量)
(4)表中Vx=4mL,t1、t2、t3的大小关系是t1<t2<t3.
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.(已知:S2O32-+2H+═H2O+S↓+SO2↑)
(1)除如图装置所示的实验用品外,还需要的一件实验用品是秒表.
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水.
(3)利用该化学反应,试简述测定反应速率的其他方法:测定一段时间内生成硫沉淀的质量(或实时测定溶液中氢离子浓度)(写一种).
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表.
(已知 I2+2S2O32-═S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
8.“碘钟”实验中,3I-+S2O82-═I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃下进行实验,得到 的数据如下表:
回答下列问题:
(1)该实验的目的是研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0sC.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比.
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1)该实验的目的是研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0sC.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比.
6.根据有机化合物的系统命名法,下列命名正确的是( )
| A. | 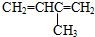 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. |  2-羟基丁烷 2-羟基丁烷 | ||
| C. |  2-乙基丁烷 2-乙基丁烷 | D. |  邻羟基苯甲酸 邻羟基苯甲酸 |
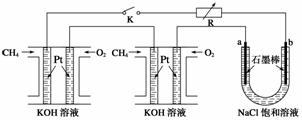 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得: