题目内容
6.在标准状况下,将O2和NO2按1:4的体积比充满干燥烧瓶,把烧瓶倒置于水中,瓶内液体逐渐上升,假设烧瓶内溶液不扩散,最终烧瓶内溶液里溶质的物质的量浓度为( )| A. | $\frac{1}{14}$ mol•L-1 | B. | $\frac{4}{5}$ mol•L-1 | C. | $\frac{1}{28}$ mol•L-1 | D. | $\frac{1}{42}$ mol•L-1 |
分析 NO2和O2按体积比4:1混合后充入一干燥烧瓶中,把烧瓶倒置于水中发生:4NO2+O2+2H2O=4HNO3,根据方程式计算.
解答 解:设混合气体中含有4VLNO2,1VLO2,则烧瓶的体积为5VL,由4NO2+O2+2H2O=4HNO3可知,恰好完全反应,气体无剩余,由N原子守恒可知,n(HNO3)=$\frac{4L}{22.4L/mol}$,c(HNO3)=$\frac{\frac{4VL}{22.4L/mol}}{5VL}$=$\frac{4}{5}$×$\frac{1}{22.4}$mol/L=$\frac{1}{28}$ mol•L-1,
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握发生的反应方程式、物质的量的相关计算公式的运用为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | X2为0.2mol/L | B. | Y2为0.2mol/L | C. | Z为0.3mol/L | D. | Z为0.45mol/L |
9.将40g镁、铁、锌组成的混合物语适量的稀硫酸恰好完全反应,蒸干溶液测得固体质量136g,在上述溶液中加入一定量的氢氧化钠溶液使金属离子全部转化为沉淀,则此沉淀的质量是( )
| A. | 96g | B. | 74g | C. | 82.5g | D. | 无法计算 |
1.亚硫酰氯(SOCl2)是一种液态化合物,沸点770C.是一种重要的化工产品.加热可发生反应4SOCl2$\frac{\underline{\;200℃左右\;}}{\;}$2SO2+S2Cl2+3Cl2(S2Cl2的沸点为138X:).工业上合成亚硫酰氯方法之一是:
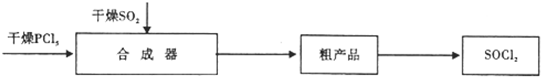
已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.

已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1取少量吸收液于试管中滴加3moL.L-1H2SO4,至溶液呈酸性,然后将所得溶液分置于A、B试管中. | 无明显现象 |
| 步骤2:在A试管中滴加紫色石蕊试液 | 若先变红后褪色,证明有ClO-,否则无 |
| 步骤3:在B试管中滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,否则无 |
11.现有H2、CO(体积比为3:2)的混合气体a L,在相同条件下,当其完全燃烧时所需O2体积为( )
| A. | 0.5 a L | B. | a L | C. | 2 a L | D. | 3 a L |
16.下列食品中富含油脂的是( )
| A. | 苹果 | B. | 大米 | C. | 白菜 | D. | 花生 |
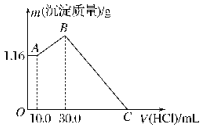 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得溶液中逐滴加入1.00mol•L-1HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得溶液中逐滴加入1.00mol•L-1HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.试回答: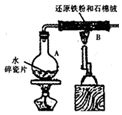 某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).
某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).