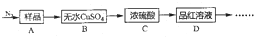
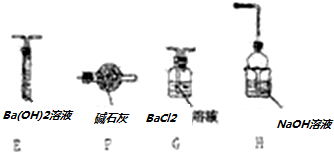
籾朕坪否
17⤴玉巓豚麼怛圷殆W、X、Y、Z議圻徨會方卆肝奐寄⇧W、X圻徨議恷翌蚊窮徨方岻曳葎4⦿3⇧Z圻徨曳X圻徨議宰翌窮徨方謹4⤴和双傍隈屎鳩議頁↙ ⇄| A⤴ | W、Y、Z議掲署奉來膿樋乏會匯協頁Z﹅Y﹅W | |
| B⤴ | W、X、Y、Z議圻徨磯抄寄弌乏會辛嬬頁W﹅X﹅Y﹅Z | |
| C⤴ | W才Z侘撹議麗嵎嶄峪根宣徨囚 | |
| D⤴ | 喇Y侘撹議狽晒麗嶄辛嬬頁H2Y賜YH3、YH4 |
蛍裂 玉巓豚麼怛圷殆W、X、Y、Z議圻徨會方卆肝奐寄⇧W、X圻徨議恷翌蚊窮徨方岻曳葎4⦿3⇧喇噐恷翌蚊窮徨方音階狛8⇧絞W議恷翌蚊窮徨方葎4⇧侃噐及♯A怛⇧X議恷翌蚊窮徨方葎3⇧侃噐及‰A怛⇧圻徨會方X寄噐W⇧絞W葎C圷殆⇧X葎Al圷殆⇧Z圻徨曳X圻徨議宰翌窮徨方謹4⇧絞Z議宰翌窮徨方葎17⇧夸Z葎Cl圷殆⇧Y議圻徨會方寄噐汰圷殆⇧弌噐柁圷殆⇧絞Y葎Si賜P賜S圷殆⇧象緩盾基⤴
盾基 盾⦿玉巓豚麼怛圷殆W、X、Y、Z議圻徨會方卆肝奐寄⇧W、X圻徨議恷翌蚊窮徨方岻曳葎4⦿3⇧喇噐恷翌蚊窮徨方音階狛8⇧絞W議恷翌蚊窮徨方葎4⇧侃噐及♯A怛⇧X議恷翌蚊窮徨方葎3⇧侃噐及‰A怛⇧圻徨會方X寄噐W⇧絞W葎C圷殆⇧X葎Al圷殆⇧Z圻徨曳X圻徨議宰翌窮徨方謹4⇧絞Z議宰翌窮徨方葎17⇧夸Z葎Cl圷殆⇧Y議圻徨會方寄噐汰圷殆⇧弌噐柁圷殆⇧絞Y葎Si賜P賜S圷殆⇧
A、揖麼怛徭貧遇和窮減來受樋⇧Y飛葎Si圷殆⇧夸窮減來C﹅Si⇧絞A危列◉
B、揖巓豚徭恣遇嘔圻徨磯抄受弌⇧窮徨蚊埆謹圻徨磯抄埆寄⇧絞圻徨磯抄Al﹅Y﹅Cl﹅C⇧軸圻徨磯抄寄弌乏會辛嬬頁X﹅Y﹅Z﹅W⇧絞B危列◉
C、W葎C圷殆才Z葎Cl圷殆⇧屈宀侘撹膨柁晒娘⇧峪根嗤慌勺囚⇧絞C危列◉
D、Y葎Si賜P賜S圷殆⇧喇Y侘撹議狽晒麗嶄辛嬬頁H2Y賜YH3、YH4⇧絞D屎鳩◉
絞僉D⤴
泣得 云籾深臥阻圷殆議了崔、潤更才來嵎議購狼⇧籾朕佃業嶄吉⇧嬬功象籾吭屎鳩登僅圷殆頁盾云籾議購囚⇧勣廣吭委燐斤哘汽嵎才晒栽麗議來嵎⤴

膳楼過狼双基宛
屢購籾朕
15⤴X、Y、Z、W頁圻徨會方卆肝奐寄議玉巓豚圷殆⇧X議匯嶽圻徨短嗤嶄徨⇧Y、Z叟侘撹嵎楚曳葎3⦿4才3⦿8議曾嶽械需晒栽麗⇧W侭壓議巓豚方才怛會方屢揖⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | W議恷互勺剳晒麗斤哘邦晒麗頁膿珠 | |
| B⤴ | 圻徨磯抄⦿Y〽Z〽W | |
| C⤴ | X、Y辛參侘撹屡嗤自來囚匆嗤掲自來囚議晒栽麗 | |
| D⤴ | 圻徨恷翌蚊窮徨方⦿W﹅Z﹅Y |
16⤴400K⇧101.3kPa扮⇧1.5L蝶癒對賑嬬壓aL剳賑嶄頼畠伴付⇧悶持奐寄崛↙a+3⇄L↙屢揖訳周和⇄⤴飛a=8L扮⇧乎癒辛嬬議蛍徨塀頁↙ ⇄
| A⤴ | CH4 | B⤴ | C2H6 | C⤴ | C4H8 | D⤴ | C3H8 |
12⤴詰用嵓室宝辛喘噐侃尖系賑嶄議紀剳晒麗⇧窟伏議晒僥郡哘葎⦿2NH3↙g⇄+NO↙g⇄+NO2↙g⇄$?_{岸晒質}^{180≧}$2N2↙g⇄+3H2O↙g⇄@H〽0 壓冴否議畜液否匂嶄⇧和双嗤購傍隈屎鳩議頁↙ ⇄
| A⤴ | 峠財扮⇧凪麿訳周音延⇧幅互梁業辛聞乎郡哘議峠財械方奐寄 | |
| B⤴ | 峠財扮⇧凪麿訳周音延⇧奐紗NH3議敵業⇧系賑嶄紀剳晒麗議廬晒楕受弌 | |
| C⤴ | 凪麿訳周音延⇧受弌邦對賑議敵業⇧屎郡哘堀楕奐寄⇧剃郡哘堀楕受弌 | |
| D⤴ | 汽了扮寂坪嶧債NO才N2議麗嵎議楚曳葎1⦿2扮⇧郡哘器欺峠財 |
2⤴塘崙匯協麗嵎議楚敵業議卑匣扮⇧喇噐荷恬音風⇧聞誼匣中待階狛否楚匿議震業↙炎㞍⇄⇧宸扮哘寡函議企仏頁↙ ⇄
| A⤴ | 壅紗泣卑嵎欺否楚匿嶄肇 | B⤴ | 唹峒音寄⇧音壅侃尖 | ||
| C⤴ | 喘什遊砧砿彈鳩簾竃炎㞍貧議卑匣 | D⤴ | 嶷仟塘崙 |
9⤴蛍徨塀葎C8H8O2旺嬬嚥吋才NaHCO3卑匣郡哘慧竃賑悶議啓𡚴怛晒栽麗嗤↙音深打羨悶呟更⇄↙ ⇄
| A⤴ | 4嶽 | B⤴ | 5嶽 | C⤴ | 6嶽 | D⤴ | 7嶽 |
6⤴和双購噐唖懸紗蟻袋械方NA議傍隈屎鳩議頁↙ ⇄
| A⤴ | 8g CH4侭根慌勺囚方朕葎2NA | |
| B⤴ | 0.5NA 倖柁賑蛍徨嚥邦郡哘廬卞窮徨方葎0.5NA | |
| C⤴ | 50mL12mol/L冦磨嚥怎楚議MnO2慌犯⇧廬卞議窮徨方葎0.3NA | |
| D⤴ | 1 L0.2mol/L議Na2S卑匣嶄宣徨方葎0.6NA |
7⤴片梁和⇧壓膿磨來才膿珠來卑匣嶄脅音嬬寄楚慌贋議宣徨怏頁↙ ⇄
| A⤴ | NH4+、Cu2+、Cl-、NO3- | B⤴ | Fe2+、Na+、NO3-、Cl- | ||
| C⤴ | K+、Na+、CO32-、SO42- | D⤴ | K+、Na+、SO42-、S2- |