题目内容
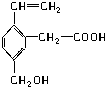 (双项)某有机物的结构如图,对这种有机物的说法正确的是( )
(双项)某有机物的结构如图,对这种有机物的说法正确的是( )| A、能使酸性KMnO4溶液褪色 |
| B、能发生酯化反应 |
| C、不能跟NaOH溶液反应 |
| D、能发生水解反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物中含碳碳双键、-COOH、-OH及苯环,结合羧酸、烯烃、醇、苯的性质来解答.
解答:
解:A.含碳碳双键,能使酸性KMnO4溶液褪色,故A正确;
B.含-OH、-COOH,可发生酯化反应,故B正确;
C.该反应含有羧基,具有酸的通性,所以能与氢氧化钠溶液发生中和反应,故C错误;
D.该分子中不含能发生水解的官能团,所以不能发生水解反应,故D错误.
故选AB.
B.含-OH、-COOH,可发生酯化反应,故B正确;
C.该反应含有羧基,具有酸的通性,所以能与氢氧化钠溶液发生中和反应,故C错误;
D.该分子中不含能发生水解的官能团,所以不能发生水解反应,故D错误.
故选AB.
点评:本题考查有机物的结构与性质,把握官能团及性质的关系为解答的关键,侧重羧酸、烯烃、醛、苯性质的考查,题目难度不大.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、因二氧化硅不溶于水,故硅酸不是二氧化硅对应的酸,或者说二氧化硅不是硅酸的酸酐 |
| B、二氧化碳通入水玻璃中得到硅酸沉淀 |
| C、二氧化硅是一种空间立体网状结构的晶体,熔点高,硬度大 |
| D、氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛放氢氟酸 |
丁烷受热分解可生成CH4、C2H6、C2H4、C3H6四者的混合气体,此混合气体对H2的相对密度是( )
| A、29 | B、14.5 |
| C、10 | D、无法确定 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1,则氢气的燃烧热(△H)为-241.8 kJ?mol-1 |
| B、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量 |
| C、己知2C(s)+2O2(g)═2CO2(g)△H=a;2C(s)+O2(g)═2CO(g);△H=b,则a>b |
| D、已知C (石墨,s)═C (金刚石,s)△H>0,则金刚石比石墨稳定 |
下列关于电解质溶液的判断正确的是( )
| A、对0.1mol/L的四种溶液H2SO4、NaOH、Na2CO3、NaCl分别加热至900C,溶液的PH都保持不变 |
| B、由0.01mol/L一元酸HA溶液的pH=4,可推知NaA溶液存在A-+H2O?HA+OH- |
| C、常温下由0.1mol/L一元碱BOH溶液的pH=12,可推知BOH溶液存在BOH=B++OH- |
| D、在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存 |
已知一定条件下一密闭容器中(各物质均为气态),1mol N2和3mol H2反应生成2mol NH3放热为Q1 kJ,下列说法正确的是( )
| A、上述反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-Q1 kJ |
| B、上述反应说明相同条件下,1 mol N2和3 mol H2 的总键能小于2 mol NH3的总键能 |
| C、相同条件下将2 mol N2和6 mol H2置于相同容器中充分反应后放出的热量为Q2kJ,Q2=2Q1 |
| D、氨水和NaOH中和反应的热化学方程式可表示为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ.mol-1 |
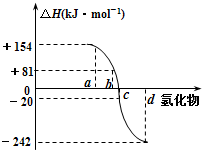 归纳整理是科学学习的重要方法之一.在学习了氧族元素的各种性质后,可整理出如下表所示部分数据和性质.请根据下表回答问题:
归纳整理是科学学习的重要方法之一.在学习了氧族元素的各种性质后,可整理出如下表所示部分数据和性质.请根据下表回答问题: