题目内容
9.现有200mLMgCl2和AlCl3的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl-)为1.3mol/L,要使Mg2+与Al3+完全分离,至少需加4mol/L的NaOH溶液的体积为( )| A. | 40mL | B. | 72mL | C. | 80mL | D. | 128mL |
分析 根据MgCl2和AlCl3的混合溶液与碱的反应可知,要使Mg2+全部转化为沉淀分离出来,Al3+恰好转化为AlO2-,先利用电荷守恒来计算Al3+的浓度,再根据反应方程式计算即可.
解答 解:MgCl2和AlCl3的混合溶液,其中Mg2+浓度为0.2mol•L-1,Cl-浓度为1.3mol•L-1,
设Al3+的浓度为x,由电荷守恒可知,
0.2mol/L×2+x×3=1.3mol/L×1,
解得x=0.3mol/L,
则将Mg2+、Al3+的物质的量分别为0.2L×0.2mol/L=0.04mol、0.2L×0.3mol/L=0.06mol,
由发生反应为MgCl2+2NaOH=Mg(OH)2↓+2NaCl
1 2
0.04mol 0.08mol
AlCl3 +4NaOH=NaAlO2+3NaCl+2H2O,
1 4
0.06mol 0.24mol
使Mg2+全部转化为沉淀分离出来,消耗的NaOH的物质的量为0.08mol+0.24mol=0.32mol,
则需加4mol•L-1NaOH溶液的体积为$\frac{0.32mol}{4mol/L}$=0.08L=80mL,
故选C.
点评 本题考查离子的分离及利用化学反应方程式的计算,题目难度中等,明确Mg2+全部转化为沉淀分离出来发生的化学反应是解答本题的关键,并注意利用氢氧化铝的两性来解答.

练习册系列答案
相关题目
12.在强碱性溶液中,可以大量共存的离子组是( )
| A. | K+、SO42-、CO32- | B. | NH4+、Na+、SO42- | C. | Mg2+、HCO3-、Cl- | D. | Ag+、Al3+、Cl- |
13.YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的超导材料,关于${\;}_{39}^{89}$Y的说法不正确的是( )
| A. | 处于第5周期 | |
| B. | 质子数与中子数之差为50 | |
| C. | 原子的核外电子数是39 | |
| D. | ${\;}_{39}^{89}$Y和${\;}_{39}^{90}$Y是两种不同的核素 |
17.在含有0.6molCl-、0.8molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.则下列正确的是( )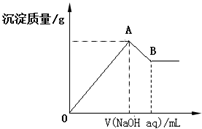

| A. | x=$\frac{3a}{5-a}$ | |
| B. | x的取值范围是0<x<$\frac{11}{32}$ | |
| C. | A点横坐标的值不随x发生变化 | |
| D. | 若B点横坐标为200mL时,c(NaOH)=7.0mol/L |
4.下列仪器:①天平;②容量瓶;③蒸馏烧瓶;④漏斗;⑤分液漏斗;⑥试管,用于分离物质的是( )
| A. | ①③④ | B. | ①②⑥ | C. | ③④⑤ | D. | ③④⑥ |
18.下列物质的溶液经加热、蒸发、浓缩、结晶、灼烧后,所得固体的成分不相同的是( )
| A. | FeCl2、FeCl3 | B. | NaHCO3、Na2CO3 | C. | NaAlO2、AlCl3 | D. | Mg(HCO3)2、MgCl2 |
19.乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:
2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g)△H=-256.1kJ•mol-1
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=-173.7kJ•mol-1.
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.
①某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1.若不使用CO,温度超过800℃,发现NO的转化率降低,其可能的原因为该反应是放热反应,升高温度反应更有利于向逆反应方向进行;在n(NO)/n(C O)=1的条件下,应控制的最佳温度在900℃左右.
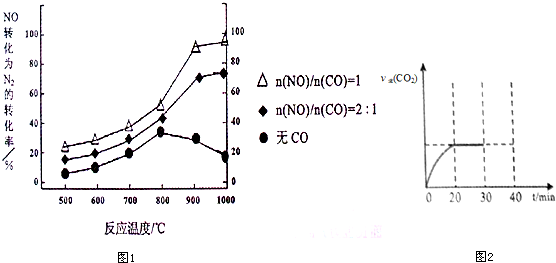
②用活性炭还原法处理氮氧化物.有关反应为:C (s)+2NO2(g)?N2 (g)+CO2 (g).某研究小组向某密闭容器中加人足量的活性炭和NO,恒温( T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
I.根据表中数据,求反应开始至20min以v(NO)表示的反应速率为0.030mol•L-1•mol-1(保留两位有效数字),T1℃时该反应的平衡常数为0.56(保留两位有效数字).
II.30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减小CO2的浓度.图2表示CO2的逆反应速率[v逆(CO2)]随反应时间的变化关系图.请在图中画出在30min改变上述条件时,在40min时刻再次达到平衡的变化曲线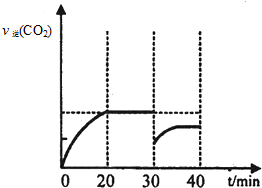 .
.
2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g)△H=-256.1kJ•mol-1
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=-173.7kJ•mol-1.
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.
①某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1.若不使用CO,温度超过800℃,发现NO的转化率降低,其可能的原因为该反应是放热反应,升高温度反应更有利于向逆反应方向进行;在n(NO)/n(C O)=1的条件下,应控制的最佳温度在900℃左右.

②用活性炭还原法处理氮氧化物.有关反应为:C (s)+2NO2(g)?N2 (g)+CO2 (g).某研究小组向某密闭容器中加人足量的活性炭和NO,恒温( T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度/mol?L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
II.30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是减小CO2的浓度.图2表示CO2的逆反应速率[v逆(CO2)]随反应时间的变化关系图.请在图中画出在30min改变上述条件时,在40min时刻再次达到平衡的变化曲线
 .
.