题目内容
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
| A、1×10-11 mol?L-1,1×10-12 mol?L-1,1×10-8 mol?L-1 |
| B、1×10-11 mol?L-1,1×10-8 mol?L-1,1×10-12 mol?L-1 |
| C、2×10-11 mol?L-1,1×10-10 mol?L-1,1×10-8 mol?L-1 |
| D、1×10-8 mol?L-1,1×10-11 mol?L-1,1×10-12 mol?L-1 |
考点:pH的简单计算
专题:
分析:根据H2O?H++OH-知,酸性溶液中,氢氧离子浓度仅由水电离产生,根据pH=-lgc(H+),结合Kw=c(H+)×c(OH-),求解溶液的c(OH-).
解答:
解:酸性溶液中,氢氧离子浓度仅由水电离产生,根据pH=-lgc(H+),常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(H+)分别为:1×10-3 mol?L-1,1×10-2 mol?L-1,1×10-6 mol?L-1,Kw=c(H+)×c(OH-)=1×10-14,
则三种物质的溶液中c(OH-)分别是1×10-11 mol?L-1,1×10-12 mol?L-1,1×10-8 mol?L-1,
故选A.
则三种物质的溶液中c(OH-)分别是1×10-11 mol?L-1,1×10-12 mol?L-1,1×10-8 mol?L-1,
故选A.
点评:本题考查了pH的简单计算,明确氢离子与氢氧根离子浓度的关系是解本题的关键,题目难度不大.

练习册系列答案
相关题目
钢铁在潮湿的空气中会被腐蚀,发生的反应为2Fe+2H2O+O2═2Fe(OH)2.以下说法正确的是( )
| A、负极发生的反应为Fe-2e-═Fe2+ |
| B、正极发生的反应为2H2O+O2+2e-═4OH- |
| C、原电池是将电能转化为化学能的装置 |
| D、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
下列物质中既能与盐酸又能与氢氧化钠溶液反应的是( )
| A、CuO |
| B、Al2O3 |
| C、Mg(OH)2 |
| D、FeCl3 |
“白色污染”的主要危害是( )
| A、破坏土壤结构 |
| B、降低土壤肥效 |
| C、污染地下水 |
| D、危及海洋生物的生存 |
25℃时,下列溶液中有关粒子的物质的量浓度关系正确的是( )
| A、pH=4的HCl溶液与pH=4的醋酸中c(Cl-)>c(CH3COO-) |
| B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸的混合溶液中c(NH4+)+c(NH3?H2O)=c(Cl-)+c(OH- ) |
| C、pH=8的0.1 mol?L-1的NaHB溶液中c(HB-)>c(H+)>c(B2-)>c (H2B) |
| D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液混合后c(HCO3-)+3c(H2CO3)-c(CO32-)=2[c(OH-)-c(H+)] |
 为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量之比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量之比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )| A、△H<0 a+b>c |
| B、△H<0 a+b<c |
| C、△H>0 a+b>c |
| D、△H>0 a+b<c |
如图所示,A、B、C、D、E是元素周期表中的5种主族元素,下列说法不正确的是( )
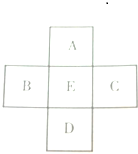

| A、A、E原子序数之差可能为2 |
| B、D、E原子序数之差可能为18或32 |
| C、B、C原子序数之差一定是2 |
| D、B、D原子序数之差不可能是7 |
下列方程式错误的是( )
| A、0.1mol?L-1CH3COOH溶液的pH为3:CH3COOH?H++CH3COO- | ||||
| B、A1Cl3溶液中加入过量稀氨水:A13++3NH3?H2O═A1(OH)3↓+3 NH4+ | ||||
C、C12与过量的铁反应:3C12+2Fe
| ||||
| D、NaHCO3溶液中加入稀盐酸:CO32一+2H+═CO2↑+H2O |
 在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图试试:
在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图试试: