题目内容
14.恒温恒压下,在一个可变容积的容器中发生如下反应:H2(g)+Br2(g)?2HBr(g)已知加入1molH2和2molBr2时,达到平衡后,生成a molHBr,(见下表“已知项”).在相同的条件下,改变起始加入情况,填写表中空白:
| 编号 | 起始状态 | 平衡时HBr物质的量(mol) | ||
| H2 | Br2 | HBr | ||
| 已知 | 1 | 2 | 0 | a |
| (1) | 2 | 4 | 0 | 2a |
| (2) | 0 | 0.5 | 1 | 0.5a |
分析 (1)反应前后气体分子数目相等,恒温恒压下,起始投料量之比与“已知”编号的相同,为等效平衡,平衡时同种物质的含相等;
(2)按化学计量数之比完全转化到左边满足氢气与溴的物质的量之比为1:2,平衡时HBr为0.5a mol,则混合气体总物质的量为“已知”编号的一半.
解答 解:(1)已知加入1molH2和2molBr2 时,达到平衡状态生成a molHBr,根据等效平衡原理:加入2molH2和4molBr2 时,反应物的起始量是原来的2倍,则平衡时HBr的量是原平衡的2倍,即HBr的物质的量为2amol,
故答案为:2a;
②若平衡时HBr的物质的量为0.5amol,则平衡时HBr的量是原来平衡HBr的物质的量的一半,所以起始时应加入0.5mol H2和1mol Br2,1molHBr转化到左边可以得到0.5mol H2和0.5mol Br2,所以还需0.5molBr2,故起始时只需加入0.5molBr2,
故答案为:0;0.5.
点评 本题考查化学平衡计算,涉及等效平衡问题,关键是理解等效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化到一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化到一边,对应物质满足等比,2:恒温恒压,按化学计量数转化到一边,对应物质满足等比.

练习册系列答案
相关题目
9.5.3g某一元醛与过量新制Cu(OH)2的碱性浊液加热充分反应,生成的红色沉淀经过滤、洗涤、烘干称其质量为7.2g,则该醛为( )
| A. | HCHO | B. | CH3CHO | C. | C5H17CHO | D. | C6H5CHO |
9.氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化.
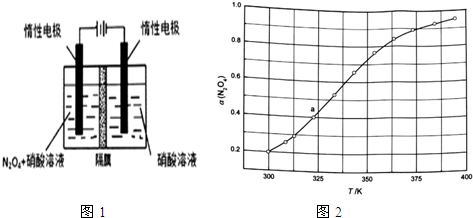
(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.
己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)?N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4.
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
设反应开始时体系压强为P0,第2.00min时体系压强为p,则p:p0=1.75;
1.00~3.00min内,O2的平均反应速率为0.090mol•L-1•min-1.
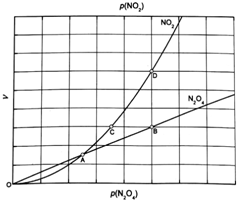
(3)从N2O4与NO2之间存在反应N2O4?2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=115.2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)?2NO2(g)是吸热反应还是放热反应,说明理由吸热反应,温度升高,α(N2O4)增加,说明平衡右移,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2(要求写出两条).
③对于反应N2O4(g)?2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2.其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=$\frac{1}{2}$K2.Kp,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).
(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.

己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)?N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4.
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
1.00~3.00min内,O2的平均反应速率为0.090mol•L-1•min-1.
(3)从N2O4与NO2之间存在反应N2O4?2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=115.2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)?2NO2(g)是吸热反应还是放热反应,说明理由吸热反应,温度升高,α(N2O4)增加,说明平衡右移,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2(要求写出两条).
③对于反应N2O4(g)?2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2.其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=$\frac{1}{2}$K2.Kp,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).

19.《常用危险化学用品贮存通则》规定:“遇火、遇热、遇潮能引起燃烧、爆炸或发生化学反应,产生有毒气体的化学危险品不得在露天或在潮湿、积水的建筑物中贮存”.下列解释事实的方程式中,不合理的是( )
| A. | 贮存液氮的钢瓶防止阳光直射:N2+O2$\frac{\underline{\;阳光\;}}{\;}$2NO | |
| B. | 硝酸铵遇热爆炸:2NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+O2↑+4H2O↑ | |
| C. | 干燥的 AlCl3遇水产生气体:AlCl3+3H2O═Al(OH)3+3HCl↑ | |
| D. | 火灾现场存有电石,禁用水灭火:CaC2→Ca(OH)2+C2H2↑ |
3.用NA表示阿伏伽德罗常数,下列叙述中正确的是( )
| A. | 0.1mol/L稀硫酸100mL中含有硫酸根个数为0.1NA | |
| B. | 200mL 1mol/L Al2(SO4)3溶液中,Al3+和SO42-离子总数为NA | |
| C. | 2.4g金属镁与足量的盐酸反应,转移电子数为2 NA | |
| D. | 标准情况下,22.4LCl2和HCl的混合气体中含分子总数为NA |
4.下列说法不正确的是( )
| A. | 实验室里易燃试剂与强氧化性试剂应分开放置并远离火源 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | 滴定实验中所用到的滴定管和移液管,在使用前均需干燥或用相应的溶液润洗,容量瓶、锥形瓶则不应润洗 | |
| D. | 将含有少量氯化钾的硝酸钾放入烧杯中,加水溶解并加热、搅拌,当溶液表面出现一层晶膜时停止加热,冷却结晶,过滤即可得到大量硝酸钾晶体 |
