题目内容
5.铁与氯化铁溶液反应时,氧化产物与还原产物的质量比是( )| A. | 2:1 | B. | 3:1 | C. | 3:2 | D. | 1:2 |
分析 发生Fe+2Fe3+═3Fe2+,只有Fe元素的化合价变化,氯化亚铁为氧化产物也为还原产物,氧化产物与还原产物的物质的量比等于质量比,以此来解答.
解答 解:铁与氯化铁溶液反应时,发生Fe+2Fe3+═3Fe2+,Fe失去电子被氧化,对应的氯化亚铁为氧化产物,Fe3+得到电子被还原,对应的氯化亚铁为还原产物,由反应可知还原剂与氧化剂的物质的量为1:2,则氧化产物与还原产物的质量比等于物质的量比,均是1:2,
故选D.
点评 本题考查氧化还原反应及计算,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化产物与还原产物的判断及守恒法应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列化学用语中,正确的是( )
| A. | 乙烯的结构简式CH2CH2 | B. | NaCl的电子式  | ||
| C. | CO2分子的结构式O-C-O | D. | Mg原子结构示意图 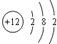 |
3.下列表示正确的是( )
| A. | 0.5mol氢 | B. | 1mol氧气 | C. | 1mole- | D. | 1mol氯化钠 |
13.“春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量,深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种,某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加入AgNO3溶液测定其浓度,所得数据如图表所示.
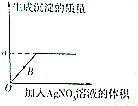 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.
(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
| 序号 | 1 | 2 | 3 | 4 | 5 |
| 每次加入AgNO溶液的体积/mL | 100 | 100 | 100 | 100 | 100 |
| 生成沉淀的质量/g | 71.75 | 143.5 | 215.25 | 287.0 | 287.0 |
 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
20.下面有关苯酚的叙述,其中正确的组合是( )
①是有机化工原料; ②易溶于水也易溶于乙醇; ③可以使紫色石蕊溶液变红; ④酸性比甲酸、乙酸、碳酸均弱;⑤不能和硝酸发生反应; ⑥常温下易被空气氧化; ⑦既可以和H2发生加成反应,又可以和溴水发生取代反应;⑧纯净的苯酚是粉红色的晶体;⑨苯酚有毒,沾到皮肤上可用浓氢氧化钠溶液洗涤;⑩苯酚能与FeCl3溶液反应生成紫色沉淀.
①是有机化工原料; ②易溶于水也易溶于乙醇; ③可以使紫色石蕊溶液变红; ④酸性比甲酸、乙酸、碳酸均弱;⑤不能和硝酸发生反应; ⑥常温下易被空气氧化; ⑦既可以和H2发生加成反应,又可以和溴水发生取代反应;⑧纯净的苯酚是粉红色的晶体;⑨苯酚有毒,沾到皮肤上可用浓氢氧化钠溶液洗涤;⑩苯酚能与FeCl3溶液反应生成紫色沉淀.
| A. | ①③⑥⑦⑧ | B. | ①②③④⑦ | C. | ①④⑥⑦ | D. | ①④⑥⑦⑩ |
10.关于有机物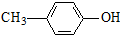 的叙述错误的是( )
的叙述错误的是( )
 的叙述错误的是( )
的叙述错误的是( )| A. | 分子式为C7H10O | B. | 含有羟基 | C. | 能发生加成反应 | D. | 含有苯环结构 |
17.下列各组单质中,在一定的条件下前者能将后者从其化合物中置换出来的是( )
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤C、Si.
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤C、Si.
| A. | 只有②④ | B. | 只有①③ | C. | 只有①②③④ | D. | ①②③④⑤ |
15.在一定条件下,可以用如图(1)所示的硼化钒(VB2)-空气电池(工作时反应为:4VB2+11O2═4B2O3+2V2O5)为电源给图(2)所示装置通电,模拟有机物的电化学储氢.下列说法正确的是( )
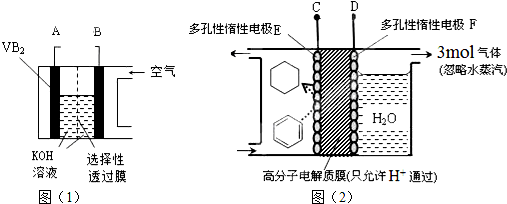

| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
 ④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉