题目内容
12.下列关于铅蓄电池的说法正确的是( )| A. | 放电时,正极电极反应是 Pb(s)+SO42-(aq)═PbSO4(s)+2e- | |
| B. | 放电时,电池的负极材料是铅板,负极质量增加 | |
| C. | 充电时,电池中硫酸的浓度始终保持不变 | |
| D. | 充电时,阳极发生的反应是 PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
分析 A.铅蓄电池放电时,正极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O;
B.放电时,负极反应式为Pb+SO42--2e-=PbSO4;
C.充电时,电池反应式为2PbSO4+2H2O=Pb+PbO2+2H2SO4;
D.充电时,阳极反应式为正极反应式的逆反应.
解答 解:A.铅蓄电池放电时,正极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,故A错误;
B.放电时,负极反应式为Pb+SO42--2e-=PbSO4,硫酸铅是固体,所以放电时负极质量增加,故B正确;
C.充电时,电池反应式为2PbSO4+2H2O=Pb+PbO2+2H2SO4,该反应中有硫酸生成,所以硫酸的浓度增大,故C错误;
D.充电时,阳极反应式为正极反应式的逆反应,所以阳极反应式为PbSO4-2e-+2H2O═PbO2+SO42-+4H+,故D错误;
故选B.
点评 本题考查原电池和电解池原理,为高频考点,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,正负极的反应与阳极、阴极的反应的逆反应,题目难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
13.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 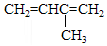 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | 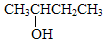 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | D. | CH3CHBrCH2CH3 2-溴丁烷 |
7.下列关于硫酸的说法正确的是( )
| A. | 浓硫酸有脱水性,故可用做干燥剂 | |
| B. | 浓硫酸有强酸性,故能与金属活动顺序氢后的金属反应 | |
| C. | 硫酸的酸性比盐酸强,利用复分解反应用硫酸可以制盐酸 | |
| D. | 由于浓硫酸具强氧化性,因此不能干燥硫化氢和碘化氢气体 |
17.下列有关金属及其合金的说法不正确的是( )
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| C. | 出土的古代铜制品表面覆盖着铜绿其主要成分为 CuO | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
4.水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
| A. | 水由液态变为玻璃态,体积一定缩小 | |
| B. | 玻璃态水不可能加工为规则的外形 | |
| C. | 玻璃态水中水分子间的作用力与冰中不完全相同 | |
| D. | 玻璃态水是分子晶体 |
1.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
2.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
| A. | 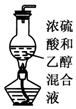 实验室制乙烯 | |
| B. | 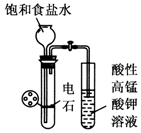 实验室制乙炔并验证乙炔能发生氧化反应 | |
| C. | 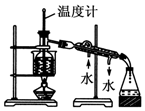 实验室中分馏石油 | |
| D. | 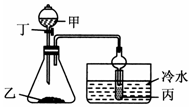 若甲为硫酸,乙为贝壳粉,丙为苯酚钠溶液,验证硫酸、碳酸、苯酚酸性的强弱 |