题目内容
2.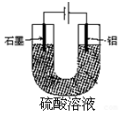 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )| A. | 阳极电极方程式为Al-3e+6OH-=Al2O3+3H2O | |
| B. | 随着电解的进行,溶液的pH逐渐增大 | |
| C. | 当阴极生成气体3.36L(标况)时,阳极增重2.4g | |
| D. | 电解过程中H+移向Al电极 |
分析 A、根据电解质为硫酸溶液可知:在阳极金属铝失去电子生成氧化铝和氢离子,不会有氢氧根离子参与反应;
B、根据电解池工作原理写出总反应,然后判断溶液的pH变化;
C、阴极生成为氢气,计算出氢气的物质的量,然后利用差量法计算出阳极增重的质量;
D、先判断电流方向,然后判断氢离子所带电荷判断氢离子的移动方向.
解答 解:A、电解质为硫酸溶液,氢氧根离子不可能参加反应,阳极反应为:Al-3e-=3Al3+,故A错误;
B、根据原电池装置和题目信息可知电解总反应为:2Al+3H2O$\frac{\underline{\;通电\;}}{\;}$Al2O3+3H2↑,水减少,溶液的pH逐渐减小,故B错误;
C、阴极反应为:2H+-2e-=H2↑,氢气的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,则转移的电子的物质的量为:2×0.15mol=0.3mol,阳极反应为:2Al+3H2O-6e-=Al2O3+6H+;根据质量差法进行计算:设阳极增重的质量为x,
2Al+3H2O-6e-=Al2O3 +6H+△m
6mol 48g
0.3mol x
6mol:0.3mol=48g:x,
解得x=2.4g,即阳极增重2.4g,故C正确;
D、根据电流方向可知,阳离子向着阴极移动,铝为阳极,石墨为阴极,所以氢离子向着石墨移动,故D错误;
故选C.
点评 本题考查电解原理、电解方程式的书写及计算,题目难度中等,注意掌握原电池、电解池工作原理,选项C为难点和易错点,注意利用差量法进行计算.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
12.化学与生产、生活密切相关,下列表述错误的是:( )
| A. | 使用新能源,减少化石燃料的燃烧,可防止酸雨的产生 | |
| B. | 光化学烟雾的形成与汽车尾气中的氮氧化物有关 | |
| C. | 建设三峡大坝使用了大量水泥,水泥是使用量最大的无机非金属材料之一 | |
| D. | “鸟巢”使用钒氮合金钢,该合金熔点、硬度和强度均比纯铁高 |
13.下列离子方程式正确的是( )
| A. | 少量AlCl3溶液滴入过量的NaOH溶液中:Al3++4OH-=AlO2-+2H2O | |
| B. | 将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+=Cu+2Na+ | |
| C. | FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ | |
| D. | 氯气溶解于水:Cl2+H2O?2H++Cl-+ClO- |
10.下列说法正确的是( )
| A. | 4mol浓盐酸与足量的二氧化锰反应生成1mol氯气 | |
| B. | 青铜是我国使用最早的合金,它的硬度和熔点都比铜的大 | |
| C. | 二氧化硅导电性能好,可用作光导纤维 | |
| D. | 液氨汽化时要吸收大量的热,可用作制冷剂 |
17.为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如图:
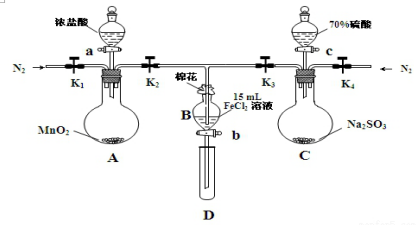
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气.
(2)棉花中浸润的溶液为氢氧化钠溶液.作用是吸收Cl2、SO2,防止污染空气
(3)A中发生反应的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)导致步骤Ⅲ中溶液变黄的离子反应是2Fe2+Cl2═2Fe3++2Cl-.用KSCN(写试剂化学式)检验氧化产物,现象是溶液变红.
(5)能说明氧化性Fe3+>SO2的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是乙丙(填“甲”“乙”“丙”).

Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气.
(2)棉花中浸润的溶液为氢氧化钠溶液.作用是吸收Cl2、SO2,防止污染空气
(3)A中发生反应的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)导致步骤Ⅲ中溶液变黄的离子反应是2Fe2+Cl2═2Fe3++2Cl-.用KSCN(写试剂化学式)检验氧化产物,现象是溶液变红.
(5)能说明氧化性Fe3+>SO2的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是乙丙(填“甲”“乙”“丙”).
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
7.胶体最本质的特征是( )
| A. | 丁达尔效应 | B. | 分散质颗粒直径在1nm~100nm之间 | ||
| C. | 布朗运动 | D. | 聚沉 |
14.下列对Na2O和Na2O2的叙述正确的是( )
| A. | 都是白色固体 | B. | 都是强氧化剂 | ||
| C. | 与酸反应的生成物都是盐和水 | D. | 都能与水反应形成强碱溶液 |
11.下列说法中,正确的是( )
| A. | SO2的摩尔质量是64 g | |
| B. | 标准状况下18 g水的体积是22.4 L | |
| C. | 14g N2含有的分子数为0.5NA | |
| D. | 1mol/LMgCl2溶液中含有Cl-的数目为2NA |
3.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素.下列说法正确的是( )
| A. | 含D的盐溶液一定显酸性 | |
| B. | 可电解熔融DE3冶炼D单质 | |
| C. | 化合物AE与CE含有相同类型的化学键 | |
| D. | 1 mol 由元素A、B组成的化合物可能含有18 mol e- |