题目内容
氮及其化合物在生活和生产等方面有重要的应用.回答下列问题:
(1)下列含氮物质属于盐的是 非电解质的是 .
A.NH3B.NH3?H2O C.NH4NO3D.HNO3E.N2
(2)写出NH4NO3电离方程式: .
(3)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是 ,所含的原子数比是 .
(4)标准状况下将 LNH3气体溶于水中,配成500mL溶液,所得氨水溶液的物质的量浓度为1mol/L.
(1)下列含氮物质属于盐的是
A.NH3B.NH3?H2O C.NH4NO3D.HNO3E.N2
(2)写出NH4NO3电离方程式:
(3)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是
(4)标准状况下将
考点:电解质与非电解质,电离方程式的书写,阿伏加德罗定律及推论
专题:
分析:(1)依据盐类的概念选择;在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不导电的化合物是非电解质,据此解答即可;
(2)NH4NO3为盐类,属于强电解质,据此书写电离方程式即可;
(3)依据阿伏伽德罗定律以及其推论回答即可;
(4)依据c=
以及n=
进行计算即可.
(2)NH4NO3为盐类,属于强电解质,据此书写电离方程式即可;
(3)依据阿伏伽德罗定律以及其推论回答即可;
(4)依据c=
| n |
| Vaq |
| V |
| Vm |
解答:
解:(1)A.NH3属于氢化物,不能电离出离子,属于非电解质;
B.NH3?H2O 属于电解质;
C.NH4NO3属于盐类;
D.HNO3电离出的阳离子全部是氢离子,属于酸;
E.N2属于单质,既不是电解质又不是非电解质;
故答案为:C;A;
(2)NH4NO3为盐类,属于强电解质,电离方程式为:NH4NO3=NH4++NO3-,故答案为:NH4NO3=NH4++NO3-;
(3)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比即是它们的物质的量之比:0.1mol:0.2mol=1:2,所含的原子数比为:(1×6):(2×4)=6:8=3:4,故答案为:1:2;3:4;
(4)500mL物质的量浓度为1mol/L的氨水,物质的量为:n=c×V=1mol/L×0.5L=0.5mol,0.5mol氨气的体积V=n×Vm=0.5mol×22.4L/mol=11.2L,故答案为:11.2.
B.NH3?H2O 属于电解质;
C.NH4NO3属于盐类;
D.HNO3电离出的阳离子全部是氢离子,属于酸;
E.N2属于单质,既不是电解质又不是非电解质;
故答案为:C;A;
(2)NH4NO3为盐类,属于强电解质,电离方程式为:NH4NO3=NH4++NO3-,故答案为:NH4NO3=NH4++NO3-;
(3)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比即是它们的物质的量之比:0.1mol:0.2mol=1:2,所含的原子数比为:(1×6):(2×4)=6:8=3:4,故答案为:1:2;3:4;
(4)500mL物质的量浓度为1mol/L的氨水,物质的量为:n=c×V=1mol/L×0.5L=0.5mol,0.5mol氨气的体积V=n×Vm=0.5mol×22.4L/mol=11.2L,故答案为:11.2.
点评:本题主要考查的是物质的量的有关计算以及盐类电离方程式书写,非电解质概念等,难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
下列各组溶液中,所含离子能大量共存的是( )
| A、K+NH4+Cl-NO3- |
| B、Cu2+H+HCO3-Cl- |
| C、Fe3+H+Cl-SCN- |
| D、Ba2+H+NO3-Fe2+ |
在下列物质中,BaSO4的溶解度最大的是( )
| A、蒸馏水 |
| B、0.5mol?L-1H2SO4溶液 |
| C、0.5 mol?L-1BaCl2溶液 |
| D、1.0mol?L-1H2SO4溶液 |
下列有关元素周期律的叙述,正确的是( )
| A、随着原子序数的递增,原子最外层电子总是从1到8重复出现 |
| B、元素的性质随着元素原子序数的递增而呈周期性变化 |
| C、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| D、元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化以及元素主要化合价的周期性变化 |
下列运用电解法生产产品的说法错误的是( )
| A、铝厂通过电解熔融氧化铝的方法冶炼铝 |
| B、制钠厂通过电解熔融氯化钠的方法生产金属钠 |
| C、用电解饱和食盐水的方法生产烧碱,同时得到氯气和氢气 |
| D、制钠厂通过电解饱和食盐水的方法生产金属钠 |

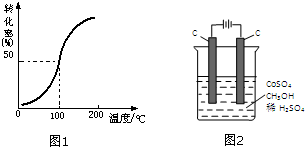 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.