题目内容
12.4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为15,W的最高价与最低价代数和为0,Y是同周期元素中离子半径最小的,Y、Z原子序数之差为4,下列说法不正确的是( )| A. | X是短周期元素中原子半径最大的 | |
| B. | X元素最高价氧化物对应的水化物,可以与其他三种元素最高价氧化物对应的水化物反应 | |
| C. | WZ4分子中每个原子最外层均达到8电子结构 | |
| D. | X元素的氧化物中只存在离子键 |
分析 4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为15,W的最高价与最低价代数和为0,则W为C元素,Y是同周期元素中离子半径最小的,Y为Al元素,Y、Z原子序数之差为4,则Z的原子序数为17号,即Z为Cl元素,原子的最外层电子数之和为15,则X的最外层电子数为15-4-3-7=1,则X为Na元素,结合元素周期律与元素化合物性质解答.
解答 解:4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为15,W的最高价与最低价代数和为0,则W为C元素,Y是同周期元素中离子半径最小的,Y为Al元素,Y、Z原子序数之差为4,则Z的原子序数为17号,即Z为Cl元素,原子的最外层电子数之和为15,则X的最外层电子数为15-4-3-7=1,则X为Na元素,
A.钠原子的半径是短周期元素中原子半径最大的,故A正确;
B.NaOH与酸和两性氢氧化物均能反应,所以与可以与其他三种元素最高价氧化物对应的水化物反应,故B正确;
C.WZ4分子即CCl4中每个原子最外层均达到8电子结构,故C正确;
D.X元素的氧化物过氧化钠中存在离子键和共价键,故D错误.
故选D.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解掌握,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10. 某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )
某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )
 某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )
某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )| A. | H2SO4浓度为4mol/L | B. | 溶液中最终溶质为FeSO4 | ||
| C. | 原混合酸中NO3-浓度为0.2mol/L | D. | AB段反应为:Fe+2Fe3+→3Fe2+ |
3.某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成.将该粉末与足量的盐酸反应有气体X逸出,X气体能被氢氧化钠溶液完全吸收.若将该粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原粉末的质量.下列判断正确的是( )
| A. | 粉末中一定有Na2O、Na2O2、NaHCO3 | |
| B. | 粉末中一定不含有Na2CO3和NaCl | |
| C. | 粉末中一定含有Na2O和NaHCO3 | |
| D. | 无法肯定粉末里是否含有NaHCO3和NaCl |
7.下列微粒在指定条件下能大量共存的一组是( )
| A. | 0.1 mol•L-1NaHCO3溶液中:C6H5O-、K+、Na+、Cl- | |
| B. | 使甲基橙显红色的溶液中:ClO-、I-、Ca2+、Mg2+ | |
| C. | 澄清透明溶液中:Al3+、S2-、NO3-、Cu2+ | |
| D. | 0.1 mol•L-1KMnO4溶液中:H+、SO32-、SO42-、Mn2+、H2C2O4 |
17.常温下,将0.1000mol•L-1NaOH溶液滴入20.0mL0.1000mol•L-1的一元酸HA溶液中,测得混合溶液的PH变化曲线如图所示,下列说法正确的是( )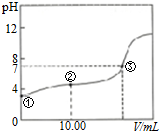

| A. | 两溶液反应的离子方程式是H++OH-+H2O | |
| B. | 图中②点所示溶液中:2c(Na+)=c(HA)+c(A-) | |
| C. | 图中②点所示溶液中:c(A-)>c(H+)>c(HA)>c(OH-) | |
| D. | 图中③点所示滴入的NaOH溶液的体积V=20.00mL |
2.下列关于碱金属的说法中,正确的是( )
| A. | 碱金属单质的密度都比水小 | |
| B. | 碱金属单质都是还原剂 | |
| C. | 碱金属单质的熔沸点一般随着原子的电子层数的增多而升高 | |
| D. | 碱金属单质在氧气中燃烧,产物都是过氧化物 |
