题目内容
5.Cl2是一种重要的化工原料,结合氯气的相关知识解决下列问题.(1)工业上将氯气通入消石灰中制取漂白粉,写出该反应的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(2)漂白粉的有效成分是(填化学式)Ca(ClO)2.
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,用离子方程式表示其原因SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2.高锰酸钾溶液常用于物质的定性检验与定量分析.某化学兴趣小组在实验室里用0.1mol/LKMnO4溶液与300ml0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为320ml.(已知MnO4-在此条件下被还原为Mn2+)
分析 (1)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成氯化钙、次氯酸钙和水;
(2)漂白粉的有效成分是次氯酸钙;
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,是因为两者发生氧化还原反应,反应的离子方程式为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;
(4)n(KI)=0.06mol,与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则n(I2)=n(KIO3)=0.02mol,结合化合价的变化计算转移的电子的数目,可计算消耗KMnO4的物质的量.
解答 解:(1)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成氯化钙、次氯酸钙和水,反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)漂白粉的有效成分是次氯酸钙,化学式为Ca(ClO)2,故答案为:Ca(ClO)2;
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,是因为两者发生氧化还原反应,反应的离子方程式为SO2+Cl2+2H2O=4H++SO42-+2Cl-
,故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;
(4)n(KI)=0.06mol,与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则n(I2)=n(KIO3)=0.02mol,共失去电子的物质的量为2×0.02mol+0.02mol×[5-(-1)]=0.16mol,则消耗KMnO4的物质的量的是$\frac{0.16mol}{7-2}$=0.032mol,所以消耗KMnO4的体积为320mL,
故答案为:320.
点评 本题考查据氯气的化学性质,学生要把握氯气的性质、氯水的成分及物质性质与用途的关系等为解答的关键,侧重分析、应用及计算能力的考查,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | c(Na+)>c(HS-)>c(K+)>c(S2-)>c(OH-)>c(H-) | B. | c(H+)>c(OH-) | ||
| C. | 2c(K+)+c(H+)═c(HS-)+2c(S2-) | D. | c(OH-)+c(S2-)=c(H+)+c(HS-)+2c(H2S) |
| A. | 原子半径:r(Y)<r(Z) | |
| B. | X和Z都只能形成一种氧化物 | |
| C. | W的最高价氧化物对应的水化物是强酸 | |
| D. | Y的简单气态氢化物的热稳定性比W的强 |
①NH4HCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3.
| A. | ②③④ | B. | ②③④⑤ | C. | ①②③④ | D. | 全部 |
Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2.
Ⅱ、某稻壳灰的成分为:
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
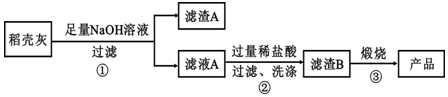
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三角架.
| A. | 不溶物一定是铜 | B. | 不溶物一定是铁 | ||
| C. | 不溶物中一定含铜,但不一定含铁 | D. | 滤液中可能含有CuSO4 |
| A. | Na2SO4和 NaCl 的物质的量之比为 1:3 | |
| B. | 溶液中一定有 1molNa2SO4 和 3molNaCl | |
| C. | 所带电荷数 SO42-是 Na+的 $\frac{3}{5}$ 倍 | |
| D. | SO42-与 Cl-的物质的量之和等于 Na+的物质的量 |
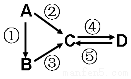 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: