题目内容
7.下列离子方程式书写正确的是( )| A. | Ba(OH)2溶液中加入少量NaHSO4:OH-+H+═H2O | |
| B. | 钠加入水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | NaOH溶液中通入足量的CO2:OH-+CO2═HCO3- | |
| D. | Al2(SO4)3溶液中加入足量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
分析 A.漏掉了钡离子与硫酸根离子生成硫酸钡沉淀的反应;
B.2mol钠与水反应生成1mol氢气,该反应不满足电荷守恒、电子守恒;
C.二氧化碳足量,反应生成碳酸氢钠;
D.氢氧化钡足量,氢氧化铝溶解.
解答 解:A.Ba(OH)2溶液中加入少量NaHSO4,反应生成硫酸钡、氢氧化钠和水,正确的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O,故A错误;
B.钠加入水中,反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.NaOH溶液中通入足量的CO2,反应的离子方程式为:OH-+CO2═HCO3-,故C正确;
D.Al2(SO4)3溶液中加入足量Ba(OH)2溶液,反应生成硫酸钡沉淀、偏铝酸钡和水,正确的离子方程式为:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
4.在强酸性无色溶液中,下列离子组能大量共存的是( )
| A. | Na+、K+、OH-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | K+、Mg2+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
15.下列说法正确的是( )
| A. | 阴离子只有还原性 | |
| B. | 含有最高价元素的化合物,只有氧化性,不具有还原性 | |
| C. | Zn和稀硫酸反应既属于离子反应,也属于氧化还原反应 | |
| D. | 没有单质参加也没有单质生成的反应一定不是氧化还原反应 |
2.用石墨电极完成下列电解实验.
下列对实验现象的解释或推测不合理的是( )
| 实验一 | 实验二 | |
| 装置 | 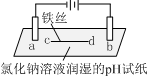 | 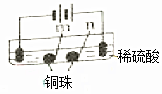 |
| 现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生;… |
| A. | a、d处:2H2O+2e-=H2↑+2OH- | |
| B. | b处:2Cl--2e-=Cl2↑ | |
| C. | 根据实验一的原理,实验二中m处能析出铜 | |
| D. | n处发生了反应:2H++2e-=H2↑ |
12.相等物质的量的下列物质,分别与足量NaOH溶液反应,消耗NaOH物质的量最多的是( )
| A. | AlCl3 | B. | Al2O3 | C. | Al(OH)3 | D. | Al |
19.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| B. | 0.5mol C2H6分子中所含C-H共价键数为2NA | |
| C. | 标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA | |
| D. | 1mol甲基-CH3所含的电子数为10NA |
17.Se是人体必需的微量元素,下列有关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的说法正确的是( )
| A. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的核外电子数不同 | |
| B. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的中子数分别为78和80 | |
| C. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质量数不同,是同种元素 | |
| D. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质子数相同,是同一种核素 |