题目内容
16.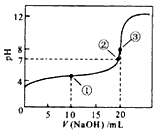 (1)常温下,用0.1000mol/LNaOH溶液滴定20.00ml 0.1000mol/L CH3COOH溶液所得滴定曲线如图.
(1)常温下,用0.1000mol/LNaOH溶液滴定20.00ml 0.1000mol/L CH3COOH溶液所得滴定曲线如图.①点①所示溶液中离子浓度由大到小排序为c(CH3COO-)>c(Na+)>c(H+)
②若二者恰好中和,则所加氢氧化钠溶液的体积等于20ml(填“大于”“小于”或“等于”)
③若用氢氧化钠溶液来滴定未知浓度的醋酸溶液,应选择酚酞做指示剂,如何判断滴定终点当滴入最后一滴氢氧化钠溶液时,溶液颜色从无色变成浅红色,且半分钟内不褪色(或不恢复原来的颜色)
(2)KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作如下所示:①称取稍多于所需量的KMnO4固体溶于水中,将溶液加热并保持微沸1h;②用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;③过滤得到的KMnO4溶液贮存于棕色试剂瓶并放在暗处;④利用氧化还原滴定方法,用基准试剂(纯度高、相对分子质量较大、稳定性较好的物质)溶液标定其浓度,KMnO4在滴定中被还原成Mn2+.请回答下列问题:
①准确量取一定体积的KMnO4溶液需要使用的仪器是酸式滴定管.
②在下列物质中,用于标定KMnO4溶液的基准试剂最好选用A(填序号).
A.H2C2O4•2H2O B.FeSO4 C.浓盐酸 D.Na2SO3
③若准确称取W g基准液试剂溶于水配成500mL溶液,取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液V mL.KMnO4溶液的物质的量浓度为$\frac{10W}{63V}$mol•L-1.
④若用放置两周后的KMnO4标准溶液去测定水样中Fe2+的含量,测得的Fe2+浓度值将偏高(填“偏高”、“偏低”或“无影响”).
分析 (1)①点①加入10mLNaOH,醋酸过量,溶液呈酸性;
②若二者恰好中和,NaOH与醋酸的物质的量相等;
③若用氢氧化钠溶液来滴定未知浓度的醋酸溶液,滴定终点呈碱性;
(2)①高锰酸钾溶液具有强氧化性,不能使用碱式滴定管,可以选用酸式滴定管量取高锰酸钾溶液;
②选做基准试剂的物质必须满足纯度高、稳定性好,如硫酸亚铁、亚硫酸钠容易被氧化变质的试剂不能作为基准试剂;
③先计算草酸的物质的量浓度,再根据草酸和高锰酸钾之间的关系式计算高锰酸钾的物质的量浓度;
④长时间放置后,高锰酸钾溶液浓度变小,滴定过程中消耗的标准液-高锰酸钾溶液的体积偏大,测定出的亚铁离子的含量偏高.
解答 解:(1)①点①加入10mLNaOH,醋酸过量,溶液呈酸性,离子浓度大小为c(CH3COO-)>c(Na+)>c(H+),
故答案为:c(CH3COO-)>c(Na+)>c(H+);
②若二者恰好中和,NaOH与醋酸的物质的量相等,因浓度相等,则体积相等,应等于20mL,故答案为:等于;
③若用氢氧化钠溶液来滴定未知浓度的醋酸溶液,滴定终点呈碱性,应滴加酚酞,达到终点时当滴入最后一滴氢氧化钠溶液时,溶液颜色从无色变成浅红色,且半分钟内不褪色 (或不恢复原来的颜色),
故答案为:酚酞;当滴入最后一滴氢氧化钠溶液时,溶液颜色从无色变成浅红色,且半分钟内不褪色 (或不恢复原来的颜色);
(2)①高锰酸钾溶液具有强氧化性,量取时应该选用酸式滴定管,
故答案为:酸式滴定管;
②硫酸亚铁、亚硫酸钠易被氧化,不稳定,浓盐酸易挥发,都易引起较大误差,只有草酸符合,故答案为:A
③草酸的物质的量浓度为:$\frac{\frac{Wg}{126g/mol}}{0.5L}$=$\frac{W}{63}$mol/L,
根据反应方程式6H++2MnO4-+5H2C2O4•2H2O═2Mn2++10CO2↑+18H2O,
2mol 5mol
c×VmL $\frac{W}{63}$mol/L×25mL
酸性高锰酸钾的物质的量浓度c=$\frac{2mol×\frac{W}{63}mol/L×25mL}{5mol×VmL}$=$\frac{10W}{63V}$mol/L;
故答案为:$\frac{10W}{63V}$mol/L;
④在放置过程中,由于空气中还原性物质的作用,使KMnO4溶液的浓度变小了,再去滴定水样中的Fe2+时,需要消耗KMnO4溶液(标准溶液)的体积会增大,导致计算出来的c(Fe2+)值会增大,测定的结果偏高,反应的离子方程式为:8H++MnO4-+5Fe2+═Mn2++5Fe3++4H2O,
故答案为:偏高.
点评 本题考查较为综合,涉及物质含量的测定以及酸碱中和的定性判断,侧重考查学生的分析能力、实验能力和计算能力,题目难度中等,明确滴定原理是解答本题的关键,注意基准试剂的选取方法,注意滴定终点现象不是褪色,而是变成紫红色.

 阅读快车系列答案
阅读快车系列答案
| A. | 1种 | B. | 3种 | C. | 4种 | D. | 2种 |
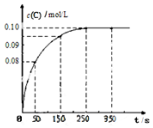 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C)随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C)随时间变化的曲线如图所示,下列说法不正确的是( )| A. | 反应在 0~50 s 的平均速率=1.6×10-3mo1/(L•s) | |
| B. | 该温度下,反应的平衡常数值为0.025 | |
| C. | 反应平衡后,再向容器中充入A、B、C各1mol,此时v(正)<v(逆) | |
| D. | 保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0 |
| A. | 在 16g18O2中含有NA个氧原子 | |
| B. | 16gCH4中含有4NA个C-H 键 | |
| C. | 22g 某气体含分子数为 0.5NA,则其摩尔质量为 44 | |
| D. | 含 NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为 1 mol•L-1 |
| A. | 平衡向正反应方向移动 | B. | x+y<z | ||
| C. | C的体积分数降低 | D. | B的转化率提高 |
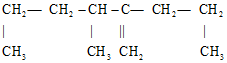 有机物,其正确命名应是( )
有机物,其正确命名应是( )| A. | 2,3-二丙基-1-丁烯 | B. | 2-丙基-3,5-二甲基-1-戊烯 | ||
| C. | 3-甲基-2-丙基-1-己烯 | D. | 3,5-二甲基-2-丙基-1-戊烯 |
| A. | 平均相对分子质量 | B. | SO3(g)的转化率 | ||
| C. | $\frac{c(S{O}_{3})}{c(S{O}_{2})}$ | D. | c2(SO3) |
| A. | H2S和SO2 | B. | O2 | C. | H2S | D. | SO3 |
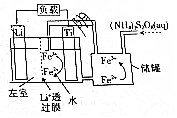
| A. | 左室电解质溶液为含Li+的水溶液 | |
| B. | 放电时,储罐中发生的离子反应为2Fe3++2SO42-═S2O82-+2Fe2+ | |
| C. | 充电时,钛极与外电源的负极相连 | |
| D. | 充电时发生的反应为Li++Fe2+$\frac{\underline{\;电解\;}}{\;}$Li+Fe3+ |