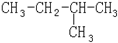题目内容
9.下列叙述中,正确的是( )| A. | 将0.l mol•L-1醋酸溶液加水稀释,溶液中所有离子的浓度都减小 | |
| B. | 0.1 mol/L的一元弱酸HA加水稀释过程中,$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$ 不变 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 中和10 mL 0.1mol•L-1醋酸与中和100 mL 0.01mol•L-1的醋酸所需同种碱液的量不同 |
分析 A.加水稀释醋酸,氢离子浓度减小,但氢氧根离子浓度增大;
B.已知Kw=c(H+)•c(OH-),Ka=$\frac{c({A}^{-})c({H}^{+})}{c(HA)}$,由$\frac{Ka}{Kw}$=$\frac{c({A}^{-})}{c(HA)c(O{H}^{-})}$;
C.醋酸是弱酸存在电离平衡,PH相同的盐酸和醋酸,醋酸溶液浓度大于盐酸;
D.10 mL 0.1mol•L-1醋酸与100 mL 0.01mol•L-1的醋酸溶液中溶质物质的量相同.
解答 解:A.加水稀释醋酸,氢离子浓度减小,温度不变溶液中离子积常数不变,氢氧根离子浓度增大,故A错误;
B.已知Kw=c(H+)•c(OH-),Ka=$\frac{c({A}^{-})c({H}^{+})}{c(HA)}$,由$\frac{Ka}{Kw}$=$\frac{c({A}^{-})}{c(HA)c(O{H}^{-})}$,已知Ka和Kw均为常数,所以$\frac{c({A}^{-})}{c(HA)c(O{H}^{-})}$不变,故B正确;
C.醋酸是弱酸存在电离平衡,PH相同的盐酸和醋酸,醋酸溶液浓度大于盐酸,中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量醋酸大于盐酸,故C错误;
D.10 mL 0.1mol•L-1醋酸与100 mL 0.01mol•L-1的醋酸溶液中溶质物质的量相同,中和10 mL 0.1mol•L-1醋酸与中和100 mL 0.01mol•L-1的醋酸所需同种碱液的量相同,故D错误;
故选B.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意酸的电离平衡常数、水的离子积常数只与温度有关,与溶液的浓度无关,题目难度中等.

练习册系列答案
相关题目
19.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核才有NMR现象.下列原子中都可产生NMR现象的是( )
| A. | 18O、31P | B. | 1H、12C | C. | 14N、23Na | D. | 24Mg、32S |
20.图是元素周期表的一部分,下列说法正确的是( )
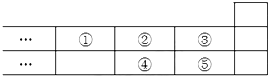

| A. | 元素①位于第二周期第IVA族 | |
| B. | 元素的最高正价是③=⑤ | |
| C. | 最高价氧化物对应水化物的酸性:③>⑤>④ | |
| D. | 气态氢化物的稳定性:④<②<③ |
17.铝材经脱脂后进行碱洗以除去氧化膜,将碱洗后的溶液中的铝以沉淀形式回收,最好加入下列试剂( )
| A. | 氨水 | B. | CO2 | C. | NaOH | D. | HNO3 |
4.下列说法或判断正确是( )
| A. | 溶剂蒸发快,得到的晶体颗粒也较大 | |
| B. | 减压过滤可过滤胶状沉淀物,且较为干燥 | |
| C. | 由0.1 mol•L-1一元碱BOH溶液的pH=10,可推知BOH溶液有BOH═B++OH- | |
| D. | 由0.1 mol•L-1一元酸HA溶液的pH=3,可推知NaA溶液有A-+H2O?HA+OH- |
10.将煤粉隔绝空气加强热,除主要得到焦炭外,还能得到如表所列的物质:
(1)表中所列物质不属于有机物的是(填序号):②⑦.
(2)能与溴水反应使之褪色的烃是(填序号):③.
(3)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为:nCH2=CH2$\stackrel{催化剂}{→}$ .
.
(4)彼此互为同系物的是(填序号):④⑤.
(5)甲苯的一氯取代产物的有4种.
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 甲烷 | 一氧化碳 | 乙烯 | 苯 | 甲苯 | 苯酚 | 氨水 |
(2)能与溴水反应使之褪色的烃是(填序号):③.
(3)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为:nCH2=CH2$\stackrel{催化剂}{→}$
 .
.(4)彼此互为同系物的是(填序号):④⑤.
(5)甲苯的一氯取代产物的有4种.
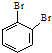 和
和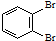
 和
和