题目内容
取1.43gNa2CO3?xH2O晶体溶于水,配成10.0mL溶液.然后逐滴加入稀盐酸直至没有气体放出为止,其用去盐酸20.0mL,并收集到标准状况下112mLCO2,试通过计算回答:
(1)稀盐酸的物质的量浓度;
(2)Na2CO3?xH2O的摩尔质量;
(3)x的值.
(1)稀盐酸的物质的量浓度;
(2)Na2CO3?xH2O的摩尔质量;
(3)x的值.
考点:化学方程式的有关计算
专题:
分析:(1)根据n=
计算二氧化碳物质的量,根据Na2CO3+2HCl=2NaCl+CO2↑+H2O计算n(HCl),再根据c=
计算盐酸物质的量浓度;
(2)由碳元素守恒n(Na2CO3?xH2O)=n(CO2),根据M=
计算Na2CO3?xH2O的摩尔质量;
(3)结合Na2CO3?xH2O的摩尔质量计算x的值.
| V |
| Vm |
| n |
| V |
(2)由碳元素守恒n(Na2CO3?xH2O)=n(CO2),根据M=
| m |
| n |
(3)结合Na2CO3?xH2O的摩尔质量计算x的值.
解答:
解:(1)二氧化碳物质的量为
=0.005mol,根据Na2CO3+2HCl=2NaCl+CO2↑+H2O可知,n(HCl)=0.005mol×2=0.01mol,盐酸物质的量浓度为
=0.5mol/L,
答:稀盐酸的物质的量浓度为0.5mol/L;
(2)由碳元素守恒n(Na2CO3?xH2O)=n(CO2)=0.005mol,Na2CO3?xH2O的摩尔质量为
=286g/mol,
答:Na2CO3?xH2O的摩尔质量为286g/mol;
(3)Na2CO3?xH2O的摩尔质量为286g/mol,则106+18x=286,故x=10,
答:Na2CO3?xH2O中x的值为10.
| 0.112L |
| 22.4L/mol |
| 0.01mol |
| 0.02L |
答:稀盐酸的物质的量浓度为0.5mol/L;
(2)由碳元素守恒n(Na2CO3?xH2O)=n(CO2)=0.005mol,Na2CO3?xH2O的摩尔质量为
| 1.43g |
| 0.005mol |
答:Na2CO3?xH2O的摩尔质量为286g/mol;
(3)Na2CO3?xH2O的摩尔质量为286g/mol,则106+18x=286,故x=10,
答:Na2CO3?xH2O中x的值为10.
点评:本题考查化学方程式计算、物质的量有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,今有如下三个热化学方程式下列关于它们的表述正确的是?( )
(1)H2(g)+
O2(g)=H2O(g)△H1=a kJ?mol-1??
(2)H2O(l)=H2(g)+
O2(g)△H2=b kJ?mol-1??
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
(1)H2(g)+
| 1 |
| 2 |
(2)H2O(l)=H2(g)+
| 1 |
| 2 |
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
| A、2b=c |
| B、b=285.8? |
| C、a=-b? |
| D、氢气的燃烧热为a kJ?mol-1 |
下列化学方程式或离子方程式正确的是( )
A、H2S在过量的O2中燃烧:2H2S+O2
| ||||
| B、向稀HNO3中加入过量的铁:Fe+4H++NO3-═Fe3++NO↑+2H2O | ||||
| C、向稀NH4HSO3溶液中滴加足量的稀NaOH溶液:NH4++OH-=NH3?H2O | ||||
| D、向氯化铝溶液滴加过量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
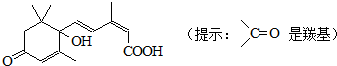
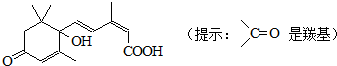
| A、含有羟基、羰基、羧基、酯基 |
| B、含有苯环、羟基、羰基、羧基 |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、含有碳碳双键、苯环、羟基、羰基 |
甲、乙两烧瓶中各盛有100mL3mol?L-1的盐酸和氢氧化钾溶液;向两烧瓶中分别加入等质量的铝粉,反应结束测得生成的气体体积甲:乙=2:3(相同状况),则加入铝粉的质量为( )
| A、2.7g | B、3.6g |
| C、5.04g | D、4.05g |
将CO2通入下列溶液中,一定不会产生沉淀的是( )
| A、Ca(OH)2溶液 |
| B、BaCl2溶液 |
| C、NaAlO2溶液 |
| D、Na2SiO3溶液 |
下列有关金属或非金属的工业制法中,正确的是( )
| A、电解饱和NaCl溶液来制备钠 |
| B、电解熔融AlCl3晶体来制备铝 |
| C、用焦炭在高温下还原二氧化硅来制备硅 |
| D、用黄铜矿(CuFeS2)直接电解精炼来制备铜 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、1mol甲苯含有6NA个C-H键 |
| B、12 g石墨和C60的混合物中质子总数一定为6NA个 |
| C、25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA |
| D、56g铁片投入足量浓硫酸中生成NA个SO2分子 |
一定质量的四种金属粉末,在足量的稀H2SO4中,生成标准状况下的氢气体积最大的是( )
| A、Na | B、Fe | C、Cu | D、Al |