题目内容
12.根据下列方程式判断下列微粒的氧化性顺序按由强到弱顺序排列的是( )2Fe2++Cl2═2Fe3++2Cl-;
2Fe3++2I-═2Fe2++I2;
I2+SO2+2H2O═4H++2I-+SO42-.
| A. | Fe3+>I2>SO2>Cl2 | B. | Cl2>Fe3+>I2>SO2 | C. | I2>Cl2>Fe3+>SO2 | D. | Cl2>SO2>I2>Fe3+ |
分析 氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,据此分析.
解答 解:反应2Fe2++Cl2═2Fe3++2Cl-中,氧化剂是Cl2,氧化产物是Fe3+,所以氧化性:Cl2>Fe3+,
反应2Fe3++2I-=2Fe2++I2中,氧化剂是Fe3+,氧化产物是I2,所以氧化性:Fe3+>I2,
反应I2+SO2+2H2O═4H++2I-+SO42-中,氧化剂是I2,还原剂是SO2,所以氧化性:I2>SO2,
综上可知,氧化性顺序为Cl2>Fe3+>I2>SO2.
故选B.
点评 本题考查氧化性强弱的判断规律:氧化剂的氧化性强于氧化产物的氧化性,注意把握氧化还原反应的基本概念,难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
5.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 分子数为NA的CO和C2H4混合气体的体积约为22.4 L | |
| B. | 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA | |
| C. | 用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA | |
| D. | 0.1 L 3.0 mol•L-1的NH4NO3溶液中含有NH${\;}_{4}^{+}$的数目为0.3NA |
3.某混合溶液中可能大量含有的离子如下表所示:
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示.
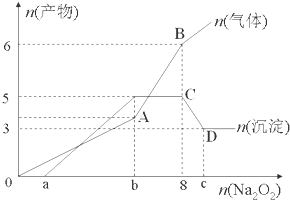
(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)a=1,b=7,c=9.
(3)写出下列离子方程式:
AB段2Na2O2+2H2O=4Na++4OH-+O2↑、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
CD段Al(OH)3+OH-=AlO2-+2H2O.
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |

(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)a=1,b=7,c=9.
(3)写出下列离子方程式:
AB段2Na2O2+2H2O=4Na++4OH-+O2↑、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
CD段Al(OH)3+OH-=AlO2-+2H2O.
20.在由水电离出的c(H+)水•c(OH-)水=10-24的溶液中一定大量共存的离子组是( )
| A. | Fe2+、Na+、NO3-、Cl- | B. | Ba2+、Na+、NO3-、Cl- | ||
| C. | SO42-、SO32-、NH4+、Na+ | D. | Mg2+、Na+、Br-、AlO2- |
7.下列各图象中,横坐标为向某溶液中加(通)入某反应物的物质的量,纵坐标为沉淀物的量,则下列叙述中正确的是( )
| A. |  向氯化铝溶液中加入过量的氨水 | |
| B. | 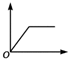 向饱和石灰水中通入过量的CO2气体 | |
| C. |  向MgCl2、AlCl3的混合液中逐滴加入NaOH溶液至过量 | |
| D. | 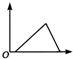 向含少量NaOH的偏铝酸钠溶液中通入过量的HCl气体 |
17.含有0.20mol碳酸钠的溶液250mL和100mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A. | 2.0mol/L | B. | 0.24mol/L | C. | 0.19 mol/L | D. | 3 mol/L |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2 L 水中含有的分子数为0.5NA | |
| B. | 标准状况下,22.4LN2中含有的原子数为NA | |
| C. | 23g Na与足量H2O反应转移的电子数为NA | |
| D. | 物质的量浓度为1 mol•Lˉ1的K2SO4溶液中,含2 NA个K+ |
2.下列说法正确的是( )
| A. | 在Ba(OH)2溶液中,c(Ba2+)=2c(OH-) | |
| B. | 蔗糖、淀粉、油脂及其水解产物均为非电解质 | |
| C. | 在难溶电解质的饱和溶液中,电解质的Ksp越小,其物质的量浓度越小 | |
| D. | 反应5S2O82-+2Mn2++8H20═10SO42-+2MnO4-+16H+,得电子的元素是氧元素,反应中转移10e- |