题目内容
阿斯匹林(aspirin)的有效成分是乙酰水杨酸,它是19世纪末合成成功的,作为一个有效的解热止痛、治疗感冒的药物,至今仍广泛使用,有关报道表明,人们正在发现它的某些新功能.阿斯匹林是由水杨酸(邻羟基苯甲酸)与乙酸酐进行酯化反应而得的.

(1)乙酰水杨酸的含氧官能团分别是 和酯基.
(2)乙酰水杨酸不应具有的性质
A、与NaOH溶液反应 B、与金属钠反应 C、与乙酸发生酯化反应 D、与乙醇发生酯化反应
(3)写出乙酰水杨酸与稀酸溶液共热的化学方程式:
(4)为测定阿斯匹林中有效成分的含量,称取样品0.250 0g,准确加入浓度为0.1015mol?L-1NaOH溶液50.00mL,煮沸60min.冷却后用浓度为0.1015mol?L-1的HC1溶液返滴过量的NaOH,消耗HC1溶液记录如下:
则该产品中乙酰水杨酸的含量为(乙酰水杨酸的摩尔质量是180.16g?mol-1.(只要求列式表示,不计算出最后结果) .

(1)乙酰水杨酸的含氧官能团分别是
(2)乙酰水杨酸不应具有的性质
A、与NaOH溶液反应 B、与金属钠反应 C、与乙酸发生酯化反应 D、与乙醇发生酯化反应
(3)写出乙酰水杨酸与稀酸溶液共热的化学方程式:
(4)为测定阿斯匹林中有效成分的含量,称取样品0.250 0g,准确加入浓度为0.1015mol?L-1NaOH溶液50.00mL,煮沸60min.冷却后用浓度为0.1015mol?L-1的HC1溶液返滴过量的NaOH,消耗HC1溶液记录如下:
| 数据 次数 | 1 | 2 | 3 |
| 初始读数 | 2.00 | 12.50 | 5.20 |
| 最后读数 | 27.10 | 37.40 | 33.20 |
考点:有机物分子中的官能团及其结构,化学方程式的有关计算,有机物的结构和性质
专题:有机反应
分析:(1)乙酰水杨酸的结构简式为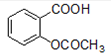 ,其含有的官能团为羧基和酯基;
,其含有的官能团为羧基和酯基;
(2)根据乙酰水杨酸中的官能团酯基和官能团羧基进行判断具有的化学性质;
(3)乙酰水杨酸在酸性条件下水解生成水杨酸和乙酸,据此写出反应的化学方程式;
(4)先计算出三次滴定消耗盐酸的体积,舍弃误差较大的数据,根据消耗的氯化氢的物质的量计算出与乙酰水杨酸反应后剩余的氢氧化钠的物质的量,然后根据乙酰水杨酸的与氢氧化钠反应方程式计算出乙酰水杨酸的物质的量,最后计算出样品中乙酰水杨酸的含量.
 ,其含有的官能团为羧基和酯基;
,其含有的官能团为羧基和酯基;(2)根据乙酰水杨酸中的官能团酯基和官能团羧基进行判断具有的化学性质;
(3)乙酰水杨酸在酸性条件下水解生成水杨酸和乙酸,据此写出反应的化学方程式;
(4)先计算出三次滴定消耗盐酸的体积,舍弃误差较大的数据,根据消耗的氯化氢的物质的量计算出与乙酰水杨酸反应后剩余的氢氧化钠的物质的量,然后根据乙酰水杨酸的与氢氧化钠反应方程式计算出乙酰水杨酸的物质的量,最后计算出样品中乙酰水杨酸的含量.
解答:
解:(1)乙酰水杨酸 中含有的官能团为羧基和酯基,故答案为:羧基;
中含有的官能团为羧基和酯基,故答案为:羧基;
(2)乙酰水杨酸中含有官能团羧基,能够与氢氧化钠溶液反应、能够与金属钠反应置换反应,也能够与乙醇发生酯化反应,但是乙酰水杨酸中不含羟基,不能与乙酸发生酯化反应,所以C正确,
故答案为:C;
(3)乙酰水杨酸与稀酸溶液共热反应生成水杨酸和乙酸,反应的化学方程式: +H2O
+H2O
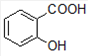 +CH3COOH,
+CH3COOH,
故答案为: +H2O
+H2O
 +CH3COOH;
+CH3COOH;
(4)第一次滴定消耗盐酸的体积为:(27.10-2.00)mL=25.10mL、第二次滴定消耗盐酸的体积为:(37.40-12.50)mL=24.90mL、第三次滴定消耗的盐酸的体积为:(33.20-5.20)mL=28.00mL,第三次得到数据误差过大,应该舍弃,第一次、第二次滴定消耗盐酸的体积为:
,根据反应关系式NaOH~HCl可知,剩余氢氧化钠的物质的量为:0.1015mol×
,乙酰水杨酸消耗的氢氧化钠的物质的量为:0.1015mol/L×50.00×10-3L-0.1015mol×
,根据反应方程式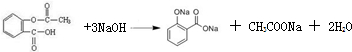 可知,乙酰水杨酸的含量为:
可知,乙酰水杨酸的含量为:
×180.16g/mol÷0.2500g×100%,
故答案为:
×180.16g/mol÷0.2500g×100%.
 中含有的官能团为羧基和酯基,故答案为:羧基;
中含有的官能团为羧基和酯基,故答案为:羧基;(2)乙酰水杨酸中含有官能团羧基,能够与氢氧化钠溶液反应、能够与金属钠反应置换反应,也能够与乙醇发生酯化反应,但是乙酰水杨酸中不含羟基,不能与乙酸发生酯化反应,所以C正确,
故答案为:C;
(3)乙酰水杨酸与稀酸溶液共热反应生成水杨酸和乙酸,反应的化学方程式:
 +H2O
+H2O | 稀硫酸 |
| △ |
 +CH3COOH,
+CH3COOH,故答案为:
 +H2O
+H2O | 稀硫酸 |
| △ |
 +CH3COOH;
+CH3COOH;(4)第一次滴定消耗盐酸的体积为:(27.10-2.00)mL=25.10mL、第二次滴定消耗盐酸的体积为:(37.40-12.50)mL=24.90mL、第三次滴定消耗的盐酸的体积为:(33.20-5.20)mL=28.00mL,第三次得到数据误差过大,应该舍弃,第一次、第二次滴定消耗盐酸的体积为:
| (24.90+25.10)×10-3L |
| 2 |
| (24.90+25.10)×10-3L |
| 2 |
| (24.90+25.10)×10-3L |
| 2 |
 可知,乙酰水杨酸的含量为:
可知,乙酰水杨酸的含量为:0.1015mol/L×50.00×10-3L-0.1015mol/L×
| ||
| 3 |
故答案为:
0.1015mol/L×50.00×10-3L-0.1015mol/L×
| ||
| 3 |
点评:本题考查了有机物官能团及结构、化学方程式的有关计算、有机物结构与性质,题目难度中等,注意熟悉常见有机物的官能团及结构,掌握常见有机物结构与性质;(4)为易错点和难点,注意掌握根据化学方程式进行计算的方法.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数相差8,A原子的最外层电子数是其次外层电子数的3倍,B单质的焰色反应为黄色.下列说法正确的是( )
| A、气态氢化物的热稳定性:A<C |
| B、元素A与B只能形成一种化合物 |
| C、最高价氧化物对应的水化物的酸性:C>D |
| D、原子半径的大小顺序:rB>rC>rD>rA |
下列过程中需要吸收热量的是( )
| A、H2→2H |
| B、2H2+O2═2H20 |
| C、CaO+H20=Ca(OH)2 |
| D、2Cl→Cl2 |
分类是日常生活、化学学习和科学研究中经常采用的一种方法.下列化学物质的分类正确的是( )
| A、碳酸钾、碳酸钙、碳酸氢钙都属于可溶性的碳酸盐 |
| B、二氧化硫、五氧化二磷、乙醇都属于氧化物 |
| C、氢氧化钡、氢氧化钾、纯碱都属于碱 |
| D、盐酸、硝酸、乙酸都属于一元酸 |
下列反应中,属于氧化还原反应的是( )
A、2 H2O2
| ||||
| B、FeO+2 HCl═FeCl2+H2O | ||||
| C、KOH+HNO3═KNO3+H2O | ||||
| D、CuCl2+2 NaOH═Cu(OH)2↓+2 NaCl |
 向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.