题目内容
下列离子方程式中书写正确的是( )
| A、铝与盐酸反应 Al+H+═Al3++H2↑ |
| B、硫酸铜与NaOH溶液反应 Cu2++OH-═Cu(OH)2↓ |
| C、铁与FeCl3溶液反应 Fe+Fe3+═2Fe2+ |
| D、硝酸银溶液与氯化钠溶液反应 Ag++Cl-═AgCl↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电子、电荷不守恒;
B.电荷不守恒;
C.电子、电荷不守恒;
D.反应生成AgCl和硝酸钠.
B.电荷不守恒;
C.电子、电荷不守恒;
D.反应生成AgCl和硝酸钠.
解答:
解:A.铝与盐酸反应的离子反应为2Al+6H+═2Al3++3H2↑,故A错误;
B.硫酸铜与NaOH溶液反应的离子反应为Cu2++2OH-═Cu(OH)2↓,故B错误;
C.铁与FeCl3溶液反应的离子反应为Fe+2Fe3+═3Fe2+,故C错误;
D.硝酸银溶液与氯化钠溶液反应的离子反应为Ag++Cl-═AgCl↓,故D正确;
故选D.
B.硫酸铜与NaOH溶液反应的离子反应为Cu2++2OH-═Cu(OH)2↓,故B错误;
C.铁与FeCl3溶液反应的离子反应为Fe+2Fe3+═3Fe2+,故C错误;
D.硝酸银溶液与氯化钠溶液反应的离子反应为Ag++Cl-═AgCl↓,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应及氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
在密闭容器中加入1molCO和1.5molH2O(气),在一定条件下达到平衡生成
molCO2,反应为CO+H2O(g)?CO2+H2,当其他条件不变,充入的水蒸气变为2mol,平衡时CO2的物质的量可能是( )
| 2 |
| 3 |
A、
| ||
| B、0.73mol | ||
| C、1mol | ||
D、
|
已知丙氨酸的结构简式为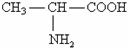 ,则下列说法不正确的是( )
,则下列说法不正确的是( )
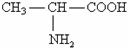 ,则下列说法不正确的是( )
,则下列说法不正确的是( )A、丙氨酸与氢氧化钠溶液反应生成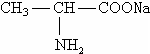 |
B、丙氨酸与盐酸反应生成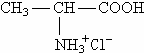 |
C、丙氨酸分子间发生成肽反应生成二肽的结构为 |
| D、丙氨酸不属于a-氨基酸 |
下列说法正确的是( )
| A、在酸性条件下,CH3CO18OC2H5水解的产物是CH3CO18OH和C2H5OH |
| B、用甘氨酸(H2NCCH2COOH)和丙氨酸(CH3CHNH2COOH)缩合,最多可形成4种二肽 |
| C、C2H5Br与NaOH的乙醇溶液混合后加热,将所得气体通入高锰酸钾酸性溶液中,若溶液褪色,则证明有乙烯生成 |
| D、将电石与饱和食盐水反应生成的气体通入溴的四氯化碳溶液中,若溶液褪色,证明有乙炔生成 |
下列气体中,既能用浓硫酸干燥,又能用氢氧化钠干燥的是( )
| A、SO2 |
| B、NO2 |
| C、H2 |
| D、NH3 |
在一定温度下,一定体积的密闭容器中,可逆反应A(S)+3B(g)?2C(g)达到平衡时,下列说法正确的是( )
①C的生成速率与C的分解速率相等
②单位时间内a mol A生成,同时消耗3a molB
③气体密度不再变化
④混合气体的总压强不再变化
⑤A、B、C的物质的量比为1:3:2
⑥混合气体的平均相对分子质量不变.
①C的生成速率与C的分解速率相等
②单位时间内a mol A生成,同时消耗3a molB
③气体密度不再变化
④混合气体的总压强不再变化
⑤A、B、C的物质的量比为1:3:2
⑥混合气体的平均相对分子质量不变.
| A、②④⑤ | B、只有① |
| C、①②③④⑥ | D、①②③④⑤ |
在一定条件下,体积为5L的密闭容器发生可逆反应2SO2+O2?2SO3,如果SO2的起始物质的量为3mol,2min后SO2的浓度为0.4mol?L-1,则用SO2的浓度变化表示的反应速率为( )
| A、1.3 mol?(L?min)-1 |
| B、0.6mol?(L?min)-1 |
| C、0.2 mol?(L?min)-1 |
| D、0.1 mol?(L?min)-1 |
下列实验操作中,仪器间不应该接触的是( )
| A、过滤时,漏斗下端管口与烧杯内壁 |
| B、使用胶头滴管时,尖嘴与试管内壁 |
| C、过滤时,盛被过滤液体的烧杯口与玻璃棒 |
| D、向试管倾倒液体药品时,试剂瓶口与试管口 |
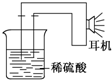 利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白: