题目内容
11.下列关于糖类、油脂、蛋白质的说法不正确的是( )| A. | 蛋白质、纤维素、蔗糖、油脂都是高分子化合物 | |
| B. | 可用浓硝酸鉴别含苯环的蛋白质 | |
| C. | 工业上利用油脂在碱的催化作用下水解生产肥皂 | |
| D. | 淀粉水解与纤维素水解得到的最终产物相同 |
分析 A.相对分子质量大于10000的属于高分子化合物;
B.含苯环的蛋白质能与浓硝酸发生颜色反应;
C.油脂在碱性条件下水解生成高级脂肪酸盐和甘油;
D.淀粉与纤维素水解最终产物是葡萄糖.
解答 解:A.蔗糖和油脂相对分子质量均较小,属于小分子化合物,故A错误;
B.某些含有苯环的蛋白质能与浓硝酸发生颜色反应,故B正确;
C.油脂在碱性条件下水解生成高级脂肪酸盐和甘油,高级脂肪酸盐为肥皂的主要成分,故C正确;
D.淀粉水解生成葡萄糖,纤维素水解液生成葡萄糖,故D正确.
故选A.
点评 本题主要考查的是常见有机化合物的鉴别、高分子化合物的概念、常见有机物的性质等,属于对基础知识的考查,题目难度不大,注意相关知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.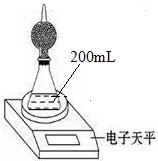 如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
①反应中生成气体的质量为1.2g.
②试计算样品中铝的质量分数?(写出计算过程)
③求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度?(写出计算过程)
 如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:| 实验操作 | t/min | 电子天平的读数/g |
| 装置+硫酸溶液 | 320.0 | |
| 装置+硫酸溶液+样品 | 0 | 335.0 |
| 1 | 334.5 | |
| 2 | 334.1 | |
| 3 | 333.8 | |
| 4 | 333.8 |
②试计算样品中铝的质量分数?(写出计算过程)
③求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度?(写出计算过程)
2.化学反应速率与化学反应限度相关知识在化工生产中应用广泛.
Ⅰ.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:
N2(g)+3H2O(g)?2NH3(g)+$\frac{3}{2}$O2(g)△H>0,进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
请回答下列问题:
(1)50℃时从开始到3h内以O2物质的量变化表示的平均反应速率为1.5×10-6mol•h-1.
(2)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢.下列措施既可增加反应速率又可以增加NH3产率的是A(填序号).
A.升高温度 B.将NH3从体系中分离
C.恒容条件下,充入He D.加入合适的催化剂
(3)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.在某10L恒容的密闭容器中加入2molN2和4molH2,达到平衡时放出的热量为92.4KJ,该条件下的平衡常数为400.下列能判断该反应一定达到平衡状态的是AD(填序号).
A.容器中气体的平均相对分子质量不随时间而变化
B.2v正(NH3)═3v逆(H2)
C.N2、H2、NH3三种物质的反应速率之比为1:3:2
D.容器中总压强不随时间而变化
E.反应的△H不再变化
Ⅱ.高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的△H<0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡.求CO的平衡转化率=60%;欲提高(2)中CO的平衡转化率,可采取的措施是C(填序号).
(3)下列措施中能使平衡时$\frac{c(CO)}{c({CO}_{2})}$增大的是D(填序号).
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的体积 F.加入合适的催化剂.
Ⅰ.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:
N2(g)+3H2O(g)?2NH3(g)+$\frac{3}{2}$O2(g)△H>0,进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
| T/℃ | 30 | 40 | 50 |
| 生成 NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
(1)50℃时从开始到3h内以O2物质的量变化表示的平均反应速率为1.5×10-6mol•h-1.
(2)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢.下列措施既可增加反应速率又可以增加NH3产率的是A(填序号).
A.升高温度 B.将NH3从体系中分离
C.恒容条件下,充入He D.加入合适的催化剂
(3)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.在某10L恒容的密闭容器中加入2molN2和4molH2,达到平衡时放出的热量为92.4KJ,该条件下的平衡常数为400.下列能判断该反应一定达到平衡状态的是AD(填序号).
A.容器中气体的平均相对分子质量不随时间而变化
B.2v正(NH3)═3v逆(H2)
C.N2、H2、NH3三种物质的反应速率之比为1:3:2
D.容器中总压强不随时间而变化
E.反应的△H不再变化
Ⅱ.高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的△H<0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡.求CO的平衡转化率=60%;欲提高(2)中CO的平衡转化率,可采取的措施是C(填序号).
(3)下列措施中能使平衡时$\frac{c(CO)}{c({CO}_{2})}$增大的是D(填序号).
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的体积 F.加入合适的催化剂.
6.下列有关化学用语使用不正确的是( )
| A. | 羟基的电子式: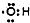 | |
| B. | 苯的分子式: | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | 甲烷分子的比例模型: |
16.某有机物的结构简式如图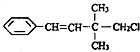 ,关于该有机物的下列叙述中不正确的是( )
,关于该有机物的下列叙述中不正确的是( )
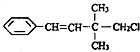 ,关于该有机物的下列叙述中不正确的是( )
,关于该有机物的下列叙述中不正确的是( )| A. | 一定条件下,能发生加聚反应 | |
| B. | 1mol该有机物在一定条件下最多能与4molH2发生反应 | |
| C. | 能使酸性KMnO4溶液、溴水褪色,且原理相同 | |
| D. | 该有机物苯环上的一溴代物有3种 |
3.下列事实中能应用勒沙特列原理来解释的是( )
| A. | 往硫化氢水溶液中加碱有利于S2-的增加 | |
| B. | 加入催化剂有利于氨氧化的反应 | |
| C. | 高压不利于合成氨的反应 | |
| D. | 500℃左右比室温更有利于合成氨的反应 |
20.下列操作过程中能出现“先产生沉淀然后又完全溶解”现象的是( )
| A. | 向CaCl2溶液中通入CO2至过量 | |
| B. | 向AlCl3溶液中滴加氨水溶液至过量 | |
| C. | 向氢氧化铁胶体中滴加稀硫酸至过量 | |
| D. | 向Na2SiO3溶液中滴加盐酸至过量 |
1.已知:①CH4(g)+2O2(g)→CO2(g)+2H2O(g)△H=-Q1kJ/mol;
②2H2(g)+O2(g)═2H2O(g)△H=-Q2 kJ/mol;
③H2O(g)═H2O(l)△H=-Q3 kJ/mol
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为( )
②2H2(g)+O2(g)═2H2O(g)△H=-Q2 kJ/mol;
③H2O(g)═H2O(l)△H=-Q3 kJ/mol
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为( )
| A. | 4Q1+0.5Q2 | B. | 4Q1+Q2+10Q3 | C. | 4Q1+2Q2 | D. | 4Q1+0.5Q2+9Q3 |