题目内容
5.写出下列物质的电子式NaOH HCl
HCl .
.
分析 NaOH含离子键和O-H共价键,由钠离子和氢氧根离子构成;
HCl只含共价键,存在共用电子对,以此来解答.
解答 解:NaOH是由钠离子和氢氧根离子构成的离子化合物,氢氧根离子中O与H以共价键相结合,其电子式为 ;
;
HCl属于共价化合物,不存在离子键,分子中氢原子与氯原子之间形成1对共用电子对,HCl电子式为 ,
,
故答案为: ;
; .
.
点评 本题考查电子式,为高频考点,把握物质的结构、构成微粒、电子式的书写方法等为解答的关键,侧重分析与应用能力的考查,注意阴离子符号的书写,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列关于能量转换的认识不正确的是( )
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 煤燃烧时,化学能主要转化为热能 | |
| C. | 绿色植物进行光合作用时,太阳能转化为化学能 | |
| D. | 白炽灯工作时,化学能主要转化为光能 |
13.下列说法正确的是( )
| A. | SO2和Cl2使品红溶液褪色的原理相同 | |
| B. | 浓硫酸分别使胆矾变白、蔗糖变黑时,浓硫酸表现的性质相同 | |
| C. | 浓硝酸和浓硫酸露置在空气中,浓度都降低的原因相同 | |
| D. | 浓硫酸与稀硫酸都能与金属锌反应放出气体,两个反应的氧化产物相同 |
20.羧酸分子里的官能团是( )
| A. | 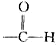 | B. | 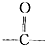 | C. | 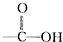 | D. | -CnHn+1 |
10.在一定温度下,某容积不变的密闭容器中,建立下列化学平衡:C (s)+H2O(g)?CO(g)+H2(g)下列叙述中可以认定上述可逆反应已达到化学平衡状态的是( )
| A. | 容器内压强不再发生变化 | |
| B. | v正(CO)=v正(H2O) | |
| C. | 生成n mol CO的同时,消耗n mol H2O | |
| D. | 1 mol H-H键断裂的同时,形成2 mol H-O键 |

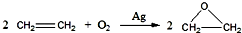
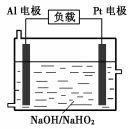 已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下:
已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下: