题目内容
6.15.6g过氧化钠粉末与足量的水蒸气和二氧化碳的混合气体接触并完全反应,固体粉末净增质量(X)和转移电子的物质的量(Y)可能是( )| A. | 5.6g、0.1mol | B. | 4.6g、0.2mol | C. | 0.3g、0.2mol | D. | 5.0g、0.4mol |
分析 求出过氧化钠的物质的量,然后根据过氧化钠与足量的水蒸气和二氧化碳的混合气体接触并完全反应的情况来分类讨论:
(1)若过氧化钠全部和水反应,根据反应可知:2Na2O2+2H2O=4NaOH+O2↑,此反应实际增重的质量是氢气的质量,且2molNa2O2~增重2mol氢气~2mol电子,据此分析;
(2)若过氧化钠全部和水反应,根据反应可知:2Na2O2+2CO2=2Na2CO3+O2↑,此反应实际增重的质量是CO的质量,且2molNa2O2~增重2molCO~2mol电子,据此分析;
通过讨论,得出两个极限值,然后取中间值即可.
解答 解:15.6g过氧化钠的物质的量为0.2mol,而过氧化钠与足量的水蒸气和二氧化碳的混合气体接触并完全反应有两种极限可能:
(1)若过氧化钠全部和水反应,根据反应可知:2Na2O2+2H2O=4NaOH+O2↑,此反应实际增重的质量是氢气的质量,且2molNa2O2~增重2mol氢气~2mol电子,故0.2mol过氧化钠能增重0.2mol氢气的质量即0.4g,转移0.2mol电子;
(2)若过氧化钠全部和水反应,根据反应可知:2Na2O2+2CO2=2Na2CO3+O2↑,此反应实际增重的质量是CO的质量,且2molNa2O2~增重2molCO~2mol电子,故0.2mol过氧化钠能增重0.2molCO的质量即5.6g,并转移0.2mol电子;
而0.2mol过氧化钠实际是和水蒸气、二氧化碳的混合气体反应,故转移的电子一定为0.2mol,而增重在0.4g到5.6g之间,故选B.
点评 本题考了过氧化钠和水、二氧化碳的范围讨论题,综合性较强,应注意的是过氧化钠和水、二氧化碳反应时,增重的分别是氢气和CO的质量,且转移的电子数相同.

练习册系列答案
相关题目
16.下表为元素周期表中短周期元素的一部分,表中所列字母分别表示一种元素.
(1)上述元素的单质中熔点最高的可能是碳(填名称).
(2)D的氢化物比G的氢化物稳定,其原因是:碳元素的非金属性比硅的非金属强.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为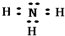 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
(4)元素C在元素周期表中位置第三周期 第IA族.
(5)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2═2Na2CO3+O2.飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2.
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
(2)D的氢化物比G的氢化物稳定,其原因是:碳元素的非金属性比硅的非金属强.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
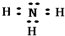 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).(4)元素C在元素周期表中位置第三周期 第IA族.
(5)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2═2Na2CO3+O2.飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2.
17.下面是一些学生的认识,其中正确的是( )
| A. | 在阴离子中,质子数一定少于核外电子数 | |
| B. | 氧化反应就是物质与氧气发生的反应 | |
| C. | 在化学反应中加入催化剂一定能加快反应的速率 | |
| D. | 最外层电子数为8的粒子一定是稀有气体元素的原子 |
1.提纯下列物质除去其中的杂质(括号中为杂质),所用试剂和方法不正确的是( )
| A. | H2SO4(HCl):AgNO3溶液、过滤 | B. | KNO3(K2SO4):Ba(NO3)2溶液、过滤 | ||
| C. | Cu(CuO):盐酸、过滤 | D. | CaCO3(CaO):水、过滤 |
3.一包由Cu、Fe、Fe2O3三种物质构成的混合粉末,某合作学习小组的同学拟探究其组成.他们称取该混合粉末20.40g放入反应器中并连接气体收集装置,向反应器逐滴加入4.00mol•L-1硫酸溶液并缓慢搅拌.当加入硫酸a mL时,混合粉末恰好完全溶解,同时收集到bL(标准状况)H2,向反应后的溶液中滴入KSCN溶液,溶液不显红色.下列结论正确的是( )
| A. | 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)=n(Fe2O3) | |
| B. | 混合粉末中物质的量之间一定满足:n(Fe)>n(Cu)>n(Fe2O3) | |
| C. | 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)═n(Fe2O3)+$\frac{bL}{22.4L•mo{l}^{-1}}$ | |
| D. | 若a=72.50,b=1.12,则20.40g混合粉末中:n(Fe)=n(Cu)=0.05mol、n(Fe2O3)=0.09mol |
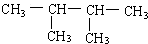 系统命名:2,3-二甲基丁烷
系统命名:2,3-二甲基丁烷
 的分子式:C4H8O
的分子式:C4H8O