��Ŀ����
�������ӷ���ʽ��д��ȷ���ǣ�������
| A���ò��缫����Ȼ�þ��Һ��2Cl-+2H2O=Cl2��+H2��+2OH- |
| B��̼��������ˮ�еĵ��룺NaHCO3=Na++H++CO3 2- |
| C��Ca��ClO��2��Һ��ͨ��SO2���壺Ca2++2ClO-+SO2+H2O=CaSO3��+2HClO |
| D��NaHSO4��Ba��OH��2��Һ��Ӧ�����ԣ�2H++SO4 2-+Ba 2++2OH -=BaSO4��+2H2O |
���㣺���ӷ���ʽ����д
ר�⣺
������A����Ӧ����������þ������������������
B��̼������Ϊǿ����ʣ�����Һ����ȫ����������Ӻ�̼��������ӣ�
C��������Ʊ�����������������ƣ�
D����Ӧ�����ҺΪ���ԣ���������������������ǡ�÷�Ӧ���������������������������ʵ���2��1��Ӧ��
B��̼������Ϊǿ����ʣ�����Һ����ȫ����������Ӻ�̼��������ӣ�
C��������Ʊ�����������������ƣ�
D����Ӧ�����ҺΪ���ԣ���������������������ǡ�÷�Ӧ���������������������������ʵ���2��1��Ӧ��
���
�⣺A���ò��缫����Ȼ�þ��Һ����Ӧ����������þ��������ȷ�����ӷ�ӦΪ��Mg2++2Cl-+2H2O
Cl2��+H2��+Mg��OH��2������A����
B��̼��������ˮ�еĵ��뷽��ʽΪ��NaHCO3=Na++HCO3-����B����
C��Ca��ClO��2��Һ��ͨ��SO2���壬���������ǿ�����ԣ��ܹ�����������������������������������Ӧ�����ӷ���ʽΪ��Ca2++2ClO-+2H2O+2SO2�TCaSO4��+SO42-+4H++2Cl-����C����
D������������Ba��OH��2��Һ��Ӧ�����ԣ���Ӧ�����ӷ���ʽΪ��2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����D��ȷ��
��ѡD��
| ||
B��̼��������ˮ�еĵ��뷽��ʽΪ��NaHCO3=Na++HCO3-����B����
C��Ca��ClO��2��Һ��ͨ��SO2���壬���������ǿ�����ԣ��ܹ�����������������������������������Ӧ�����ӷ���ʽΪ��Ca2++2ClO-+2H2O+2SO2�TCaSO4��+SO42-+4H++2Cl-����C����
D������������Ba��OH��2��Һ��Ӧ�����ԣ���Ӧ�����ӷ���ʽΪ��2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����D��ȷ��
��ѡD��
���������⿼�������ӷ���ʽ����д�жϣ�Ϊ�߿��ĸ�Ƶ�⣬�����е��Ѷȵ����⣬ע����ȷ���ӷ���ʽ�����жϳ��÷������磺��鷴Ӧ��������Ƿ���ȷ���������ʲ���Ƿ���ȷ���������������ʵ���Ҫ������ѧʽ������Ƿ����ԭ��ѧ����ʽ�ȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
����������ȷ���ǣ�������
| A��̼����Ԫ������Ȼ���о����ڶ���ͬ�������� |
| B��ϡ�����ˮϡ�ͣ��������̶�������Һ��pH��С |
| C����ʯ��ˮ�м�������CaO�����ָ������º���Һ��pH���� |
| D����ͬ�����£�2 mol��ԭ�������е���������l mol����������е����� |
���и��������в����ڵȵ�������ǣ�������
| A��CO2��N2O |
| B��O3��SO3 |
| C��CO32-��NO3- |
| D��CH4��NH4+ |
ˮ��Һ���ܴ��������һ�������ǣ�������
| A��K+��Al3+��Cl-��CO32- |
| B��H+��Na+��Br-��SiO32- |
| C��Na+��Fe2+��SO42-��NO3- |
| D��K+��NH4+��OH-��NO3- |
��������������Ӧ�õ������ϵ��ȷ���ǣ�������
| A����̿����ǿ��ԭ�ԣ��������ܽ��������軹ԭΪ�� |
| B����������������뵼������������۵�ߡ�Ӳ�ȴ� |
| C���������̾���ǿ�����ԣ����ܽ�˫��ˮ����Ϊ���� |
| D��Fe��Cu���ã�����FeCl3��Һ���Ը�ʴ��·���ϵ�Cu |
��֪���������ˮ�еĵ���ƽ�ⳣ����25�棩���±���
������0.1mol?L-1�ģ�NH4��2CO3��Һ�����д�����ǣ�������
| ������� | H2CO3 | NH3?H2O |
| ����ƽ�ⳣ�� | Ka1=4.30��10-7 Ka2=5.61��10-11 | 1.77��10-5 |
| A��c ��NH4+����c ��CO32-����c ��NH3?H2O����c ��HCO3-�� |
| B��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+2 c��CO32-�� |
| C��c ��CO32-��+c ��HCO3-��+c ��H2CO3��=0.1 mol?L-1 |
| D��c ��NH4+��+c ��NH3?H2O��=2 c ��CO32-��+2c ��HCO3-��+2 c ��H2CO3�� |
�����й����ʵ��Ʊ�����������������ȷ���ǣ�������
| A��ͨ����������Һ�м���������NaOH��Һ�����Ʊ�Al��OH��3 |
| B��ͨ���������ʯ��ˮ������Na2CO3��Һ��NaHCO3��Һ |
| C������ͨ��ɫ��Ӧ����ɫ��ͬ������FeCl3��Һ��FeCl2��Һ |
| D��ֻ�����������NaOH��Һ���ٹ��ˣ����ܳ�ȥFe2O3�е�Al2O3 |
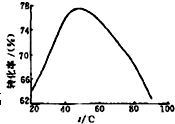 ����ʯ����������������þ����Ҫ�����������£�
����ʯ����������������þ����Ҫ�����������£�


 ��һ;���⣬��һ;�����ɵ��м����Ľṹ��ʽΪ
��һ;���⣬��һ;�����ɵ��м����Ľṹ��ʽΪ