题目内容
根据化学反应的本质并根据下列数据信息讨论判断:氢气燃烧生成水蒸气时,是释放能量还是吸收能量?

解析:
|
导思:在学习了从2个角度分析放热反应和吸热反应后,依据化学反应的本质——就是旧化学键断裂和新化学键的形成过程,要知道破坏旧化学键是否需要吸收一定的能量来克服原子或离子之间的相互作用;形成新化学键时,是否要释放一定的能量.而判断放热反应还是吸热反应的关键是看旧键断裂和新键形成2个过程的综合结果. 如果反应物旧化学键的断裂吸收的能量小于生成物新化学键的形成释放的能量,则反应为放热反应;反之为吸热反应. 探究:通过计算来探究:从化学键的角度考查了放热反应和吸热反应.上述反应中的能量变化应该是断裂1 mol H2的共价键和0.5 mol O2的共价键吸收的总能量与形成1 mol H2O的共价键释放的总能量的代数和.通过计算可知,氢气燃烧生成水蒸气时,是放出能量. |

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案美籍埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而获得1999年诺贝尔化学奖.激光有很多用途,例如波长为 m的红外激光能切断
m的红外激光能切断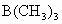 分子中的一个B—C键,使之与HBr发生取代反应[
分子中的一个B—C键,使之与HBr发生取代反应[ 分子中一个—
分子中一个—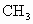 基团被Br原子所代替]:
基团被Br原子所代替]:

而利用9.6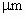 的红外激光却能切断两个B—C键,并与HBr发生二元取代反应.
的红外激光却能切断两个B—C键,并与HBr发生二元取代反应.
(1)观察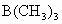 的分子式并根据原子结构理论,试推断三个B—C键之间的键角是多少
的分子式并根据原子结构理论,试推断三个B—C键之间的键角是多少
 [ ]
[ ]
|
A. |
B. |
|
C.90° |
D.120° |
(2)B原子最外电子层是否达到8电子稳定结构?
_____________________________________.
(3)从这个实验中可以看出化学反应的本质是_____________________________________.
(4)试写出二元取代的化学方程式:_____________________________________.
(5)现用5.6g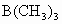 和
和 g
g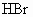 正好完全反应,则生成物中除了甲烷外,其他两种产物的物质的量之比为多少?
正好完全反应,则生成物中除了甲烷外,其他两种产物的物质的量之比为多少?
 ,分子中的一个B—C键,使之与HBr发生取代反应(
,分子中的一个B—C键,使之与HBr发生取代反应(
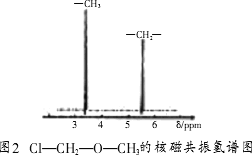
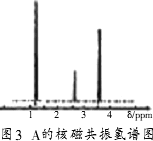

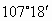
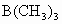 ,分子中的一个B—C键,使之与HBr发生取代反应(
,分子中的一个B—C键,使之与HBr发生取代反应(