题目内容
实验中不能直接测出由石墨和氢气生成甲烷反应的反应热,但可测出CH4、石墨和H2的燃烧热。试求出石墨生成甲烷的反应热。
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.5kJ·mol-1;
C(石墨)+O2(g)= CO2(g) △H2=-393.5kJ·mol-1 ;
H2(g)+1/2O2(g)= H2O(l) △H3=-285.8kJ·mol-1。
求:C(石墨)+ 2H2(g)= CH4(g)△H4
【答案】
-74.6 kJ·mol-1
【解析】试题分析:利用盖斯定律计算热化学方程式的加减。反应物为1mol的石墨和2mol的氢气,所以△H4=-393.5+(-285.8×2)-(-890.5)=-74.6kJ·mol-1
考点:学习根据间接的反应判断总反应的反应热。
点评:在用盖斯定律计算时,要准确找到反应物和生成物及它们的量。这样有助于能准确的对已知方程进行乘除,到最终的加和。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 O2(g)=H2O(l) ΔH3=-285.8kJ?mol-1
O2(g)=H2O(l) ΔH3=-285.8kJ?mol-1
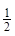 O2(g)=H2O(l) ΔH3= ─285.8 kJ?mol-1
O2(g)=H2O(l) ΔH3= ─285.8 kJ?mol-1
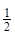 O2(g)=H2O(l)
ΔH3= ─285.8 kJ?mol-1
O2(g)=H2O(l)
ΔH3= ─285.8 kJ?mol-1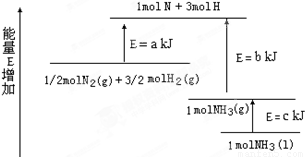
 如果有1molN2 完全反应,要吸收热量68kJ.写出该反应的热化学方程式______________________________________________.
如果有1molN2 完全反应,要吸收热量68kJ.写出该反应的热化学方程式______________________________________________.