题目内容
下列离子方程式书写正确的是
A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:
2H+ + SO42- + Ba2+ + 2OHOHOHOH- = BaSO4↓+ 2H2O
B.将标准状况下112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中:
2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 6Cl- + 2Br2
C.用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O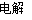 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.向澄清石灰水中加入过量的碳酸氢钠溶液: Ca2+ + OHOHOHOH- + HCO3-= CaCO3↓ + H2O
A
【解析】
试题分析:NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性,说明H+与OH-恰好反应,A正确;标况下112 mL氯气的物质的量为0.005moL, 10 mL 1 mol·L-1的溴化亚铁溶液的物质的量为0.01moL,比值为1:2,氧化性排序为:Cl2>Br2>Fe3+>I2,发生反应Cl2+2Fe2+=2Cl-+2Fe3+,B错误;Mg(OH)2难溶于水,所以用惰性电极电解饱和MgCl2溶液应为:Mg2++2Cl-+2H2O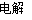 Cl2↑+H2↑+2Mg(OH)2↓,错误;根据“以少定多”的原则,向澄清石灰水中加入过量的碳酸氢钠溶液,石灰水完全反应,离子方程式为:Ca2+ +2 OHOHOHOH- +2HCO3-= CaCO3↓ +2H2O + CO32-,D错误。
Cl2↑+H2↑+2Mg(OH)2↓,错误;根据“以少定多”的原则,向澄清石灰水中加入过量的碳酸氢钠溶液,石灰水完全反应,离子方程式为:Ca2+ +2 OHOHOHOH- +2HCO3-= CaCO3↓ +2H2O + CO32-,D错误。
考点:考察离子方程式的正误判断。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
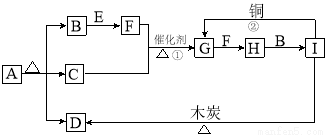
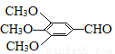 )和抗癫痫药物H(
)和抗癫痫药物H(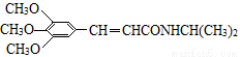 )的路线如下(部分反应略去条件和试剂):
)的路线如下(部分反应略去条件和试剂): 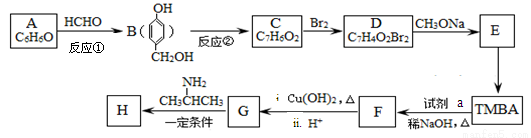
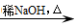
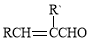 + H2O(R、R’表示烃基或氢)
+ H2O(R、R’表示烃基或氢)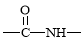 )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。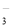 + Ca2+ + OH- = CaCO3↓ + H2O
+ Ca2+ + OH- = CaCO3↓ + H2O = Fe3++ NO↑ + 2H2O
= Fe3++ NO↑ + 2H2O 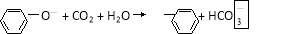

 ____Cu+____CuCl2+____N2↑+____H2O。
____Cu+____CuCl2+____N2↑+____H2O。