题目内容
下列说法正确的是( )
| A、强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子 |
| B、强电解质的水溶液导电性强于弱电解质的水溶液 |
| C、强电解质都是离子化合物,弱电解质都是共价化合物 |
| D、强电解质易溶于水,弱电解质难溶于水 |
考点:弱电解质在水溶液中的电离平衡,强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A、强电解在水溶液中完全电离,而弱电解质在水溶液中部分电离;
B、溶液的导电能力与离子的浓度有关,与电解质的强弱无关;
C、有些强电解质为共价化合物,有些弱电解质为离子化合物;
D、电解质的强弱与溶解性无关.
B、溶液的导电能力与离子的浓度有关,与电解质的强弱无关;
C、有些强电解质为共价化合物,有些弱电解质为离子化合物;
D、电解质的强弱与溶解性无关.
解答:
解:A.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,而弱电解质在水溶液中部分电离,故A正确;
B.溶液的导电能力与离子的浓度有关,浓度越大导电能力越强,浓度越小导电能力越弱.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物,溶液的导电能力与电解质的强弱无关,如硫酸钡是强电解质,难溶于水,离子浓度小,导电能力弱,CH3COOH为弱电解质,易溶于水,当乙酸浓度比较大时,离子的浓度大,导电能力强,故B错误;
C.氯化氢为强电解质,但氯化氢为共价化合物,故C错误;
D.电解质的强弱与溶解性无关,故D错误.
故选A.
B.溶液的导电能力与离子的浓度有关,浓度越大导电能力越强,浓度越小导电能力越弱.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物,溶液的导电能力与电解质的强弱无关,如硫酸钡是强电解质,难溶于水,离子浓度小,导电能力弱,CH3COOH为弱电解质,易溶于水,当乙酸浓度比较大时,离子的浓度大,导电能力强,故B错误;
C.氯化氢为强电解质,但氯化氢为共价化合物,故C错误;
D.电解质的强弱与溶解性无关,故D错误.
故选A.
点评:本题考查了导电能力大小与强弱电解质的关系,难度不大,注意“导电能力大小与离子浓度有关,与电解质强弱无关”是解答本题的关键.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
下列分子的电子式书写正确的是( )
A、氨气  |
B、四氯化碳  |
C、氮气  |
D、二氧化碳  |
下列化工方法不属于化学变化的是( )
| A、分馏 | B、裂化 | C、裂解 | D、干馏 |
几种短周期元素的原子半径及主要化合价如表,下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、Y最高价氧化物对应的水化物的碱性强于X |
| B、一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C、Y与W形成的化合物具有两性,能溶于浓氨水 |
| D、Y与Z的最高价氧化物对应的水化物能相互反应 |
某有机物的结构简式如图,有关它的说法正确的是( )
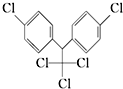

| A、它属于芳香烃 |
| B、该有机物不含官能团 |
| C、分子式为C14H8Cl5 |
| D、1mol该物质能与6mol H2加成 |
下列叙述中,正确的是( )
| A、1 mol H2的质量只有在标准状况下才约为2 g |
| B、1 mol H2和O2的混合气体,在标准状况下的体积也是约为22.4L |
| C、在20℃时,1 mol的任何气体的体积总比22.4 L大 |
| D、标准状况下SO3的体积是22.4L时,则其物质的量约是1 mol,所含分子数约是6.02×1023 |
下列叙述正确的是( )
| A、ⅠA族元素单质的熔点从上往下逐渐降低 |
| B、分子晶体中一定存在共价键 |
| C、ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| D、同周期非金属氧化物对应的水化物的酸性从左往右依次增强 |
下列叙述正确的是( )
| A、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃 |
| B、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃的含氧衍生物 |
| C、某有机物燃烧后产物只有CO2和H2O,通过测定有机物、CO2和H2O的质量,可确定有机物是否含有氧 |
| D、甲烷在同系物中含碳量最高,因而是清洁能源 |
 为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题: