题目内容
11.四份相同质量的铝与足量下列物质发生反应,能放出氢气且消耗溶质物质的量最少的是( )| A. | 稀硫酸 | B. | 稀硝酸 | C. | 盐酸 | D. | 氢氧化钠溶液 |
分析 首先硝酸与金属铝反应不生成氢气,根据生成物的化学式:Na[Al(OH)4]、Al2(SO4)3、AlCl3,通过物料守恒可直接判断出等量的铝消耗NaOH物质的量最少.
解答 解:设Al为1mol,
A.铝与稀硫酸反应生成Al2(SO4)3,1mol铝消耗1.5mol硫酸;
B.硝酸与金属铝反应不生成氢气,
C.铝与盐酸反应生成AlCl3,1mol铝消耗3mol盐酸;
D.铝与氢氧化钠溶液反应生成Na[Al(OH)4],1molAl消耗1molNaOH;
综合以上分析可知放出氢气且消耗溶质物质的量最少的是氢氧化钠溶液,
故选D.
点评 本题考查铝的性质,侧重于物质的量的判断,解答时可根据生成物的化学式,从质量守恒的角度分析,易错点为B,注意硝酸与铝反应不生成氢气,题目难度不大.

练习册系列答案
相关题目
19.用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A. | 标准状况下,22.4LSO3含有的分子数NA | |
| B. | 常温常压下,4.4gCO2的物质的量一定为0.1mol | |
| C. | 标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L | |
| D. | 7.8gNa2S和7.8gNa2O2中含有的阴离子数目均为0.1NA |
6.下列反应的离子方程式正确的是( )
| A. | 向Al2(SO4)3溶液中逐滴滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| B. | 用惰性电极电解熔融氯化钠:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 硫化钠发生水解:S2-+2H2O═H2S+2OH- | |
| D. | 向NH4HSO4溶液中加入NaOH溶液至混合液呈中性:H++OH-═H2O |
3.下列关于原子结构和元素周期律的说法,正确的是( )
| A. | 原子核内质子数为15的元素的最高正价为+3 | |
| B. | 电子层数相同时,最外层7个电子的元素非金属性最强 | |
| C. | 原子序数从11依次增加到17,原子半径逐渐增大 | |
| D. | 随着原子序数的增加,元素原子最外层电子数逐渐增多 |
20.下列实验操作不正确的是( )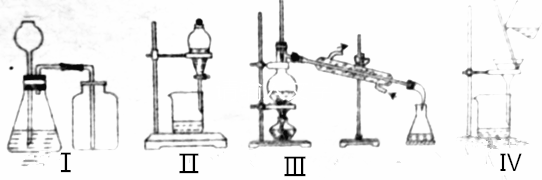

| A. | 选择装置Ⅰ用铜与浓硝酸反应制备NO2 | |
| B. | 选择装置Ⅱ分离乙酸乙酯和饱和碳酸氢钠溶液的混合物 | |
| C. | 选择装置Ⅲ分离对硝酸甲苯和邻硝基甲苯 | |
| D. | 选择装置Ⅳ分离饱和硫代硫酸钠溶液和硫代硫酸钠晶体的混合物 |
2.温度为T时,向4L恒容密闭容器中充入2molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g),经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A. | 反应在前50s的平均速率为v(PCl3)=0.0064mol/(L•s) | |
| B. | 保持其它条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入4molPCl3、4molCl2,达到平衡时,则此反应的化学平衡常数为0.025mol/L | |
| D. | 相同温度下,起始时间向容器中充入2molPCl5、0.40molPCl3和0.40molCl2,达到平衡前v(正)<v(逆) |
