题目内容
4.对于H3O+的下列说法中正确的是( )| A. | O原子采用SP2杂化 | B. | O原子采用SP3杂化 | ||
| C. | O原子采用SP杂化 | D. | 离子中存在非极性 |
分析 H3O+中氧原子含有3个共价单键和一个孤电子对,根据价层电子对互斥理论确定其空间构型,价层电子对数=σ 键个数+$\frac{1}{2}$(a-xb);H3O+是H+与H2O通过配位键形成;H3O+离子中不存在非极性键,存在的都是H-O极性共价键.
解答 解:H3O+中氧原子含有3个共价单键和一个孤电子对,水合氢离子中氢离子含有空轨道,氧原子含有孤电子对,所以二者形成一个配位键,结构式为: .
.
A.H3O+中,价层电子对数=3+$\frac{1}{2}$(6-1-3×1)=4,在H3O+中O原子成3个σ键,其中含有1个配位键,有一对未成键的孤对电子,杂化轨道数为4,采取sp3型杂化杂化,故A错误;
B.由A项分析可知O原子采用SP3杂化,故B正确;
C.由A项分析可知O原子采用SP3杂化,故C错误;
D.H3O+离子中不存在非极性键,存在的都是H-O极性共价键,故D错误.
故选:B.
点评 本题考查了杂化理论的应用、共价键的极性,题目难度不大,注意理解价层电子对互斥理论与杂化轨道理论,为高频考点.

练习册系列答案
相关题目
14.下列关于铜电极的叙述正确的是( )
| A. | 铜锌原电池中铜是正极 | |
| B. | 用电解法精炼铜时粗铜作阴极 | |
| C. | 在电解饱和CuCl2溶液时,用铜作阳极 | |
| D. | 电解饱和食盐水时,用铜片作阳极 |
15. 某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
(1)称取13.0 g草酸晶体,配成250 mL水溶液.此操作过程必须用到的2种定量仪器是托盘天平和250mL容量瓶.
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①配平离子方程式:MnO${\;}_{4}^{-}$+H2C2O4+H+→Mn2++CO2↑+H2O
②滴定达到终点的标志是加入最后一滴高锰酸钾溶液,锥形瓶内溶液由无色变为红色,且半分钟不褪色.
(3)按正确操作测得有关数据记录如下:
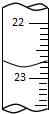
①a的读数如图所示,则a=22.80;
②草酸晶体的纯度为98.86%(结果保留两位小数).
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏低的是C.
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
 某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:(1)称取13.0 g草酸晶体,配成250 mL水溶液.此操作过程必须用到的2种定量仪器是托盘天平和250mL容量瓶.
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①配平离子方程式:MnO${\;}_{4}^{-}$+H2C2O4+H+→Mn2++CO2↑+H2O
②滴定达到终点的标志是加入最后一滴高锰酸钾溶液,锥形瓶内溶液由无色变为红色,且半分钟不褪色.
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 草酸溶液体积 | 酸性KMnO4溶液体积 | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.20 | 20.58 |
| 第二次 | 25.00 | 4.00 | 24.40 |
| 第三次 | 25.00 | 2.38 | a |
②草酸晶体的纯度为98.86%(结果保留两位小数).
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏低的是C.
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
12.下列离子方程式中,错误的是( )
| A. | 将氨通入盐酸中:NH3+H+=NH4+ | |
| B. | 在稀NaOH溶液中滴入几滴NH4Cl溶液:NH4++OH-=NH3↑+H2O | |
| C. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
19.将Mg、Cu组成的26.4g混合物投入到适量的稀硝酸中,固体完全溶解,将产生的气体和6.72L(标准状况下)氧气混合通入水中,恰好全部被水吸收.向反应后的溶液中加入足量4mol/L-1的NaOH溶液,使金属离子完全沉淀.则形成沉淀的质量是( )
| A. | 63.8 g | B. | 53.6 g | C. | 46.8 g | D. | 43.2 g |
9.某温度时,浓度都是1mol/L的两种气体X2、Y2在密闭容器中反应生成气体Z达平衡后,c (X2)为0.4mol/L,c (Y2)为0.8mol/L,生成c (Z)为0.4mol/L,则该反应的反应式(z用x、y表示)是( )
| A. | X2+2Y2 ?2XY2 | B. | 2X2+Y2 ?2X2Y | C. | 3X2+Y2?2X3Y | D. | X2+3Y2?2XY3 |
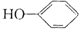 合成
合成 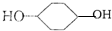
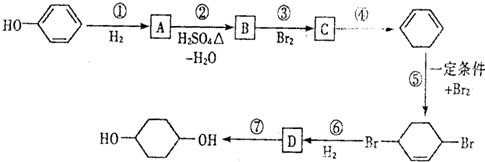
 ,D
,D .
.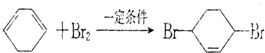 写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式
写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式 .
. 的反应方程式(有机物写结构简式,注明反应条件).
的反应方程式(有机物写结构简式,注明反应条件). .
.